Master's Perspective
人工肝臓・部分肝移植・そして肝細胞脾臓内移植へ
〜肝機能の再建(再生)を志した40年の歩み〜
水戸 廸郎
旭川医科大学名誉教授
はじめに
私は1956年、インターンを終え、北海道大学医学部第一外科の新制大学院一期生として入学(局)した。爾来、北大に約20年、その間に2年間の外国留学を経験して、‘75年に新設の旭川医科大学 第2外科教室を主催し、‘98年に退官するまで40年にわたりAcademic Surgeonとして研究の現場に在籍した。
その間の研究対象は一貫して肝臓であり、自分なりに職責を果たし、成果を挙げたと自負している。しかし、研究の場を離れると成果に対する諸々の課題が浮上する。これらを提起することで、現在から未来にわたり活躍を期待されている肝臓研究者の方々に「他山の石」、換言するなら「温故知新」飛躍の糧の一助になればと希望し、あえて、科学随筆風に私共の成果を振り返りみることにする。
1.肝臓外科との出会い;無からの人工肝臓開発
現在では肝切除手術は消化器(肝、胆、膵)外科専門医なら誰でもメスを取れるほどに一般化し、普及している。しかし、1950年代、本邦では2、3の大学で施行されているに過ぎず、私が入局した教室の 故三上 二郎教授はその年の第56回日本外科学会総会で[肝広汎切除]の宿題報告を終えた時であった。現在は行われていないが、宿題報告は時代の先端的課題を会長が依頼し、担当教室を挙げて基礎、臨床研究に取り組み、その成果が広く普及することを意図したものであった。否応なしに私の研究課題は肝臓外科になり、指導教官は 故葛西 洋一筆頭助手(後の4代目教授)に決められた。
まず、読むようにと手渡された本はH. Gans著 Introduction to HEPATIC SURGERY(1955年260頁)であり、初めて手にした洋書、初めて知るGlisson系分岐による肝臓の区域、区域脈管処理後の切除術などであった。更に、一夜にして食いちぎられた肝臓が元に復するとしたギリシャ神話が19世紀末、犬の肝4/5切除後6週で術前重量になることが近代科学手法で既に確認されていることを知り、自分の知識の無さを痛感した。加えて、切除量は肝臓の[Reserve Capacity]によるとする実験研究の報告などが明記され、硬変合併肝癌に対しての広範囲切除に警鐘を鳴らしている。これらの報告を知ってか知らずに70〜80年代にかけ肝予備力、硬変合併肝癌切除の多くの報告や論議が日本外科学会学術集会などで行われたが、現在は予備力の基準として簡便なChild-Pugh分類が広く使用されている。いずれにせよ、他の臓器には見られない「肝再生」が私の終生の研究課題となった(図1)。
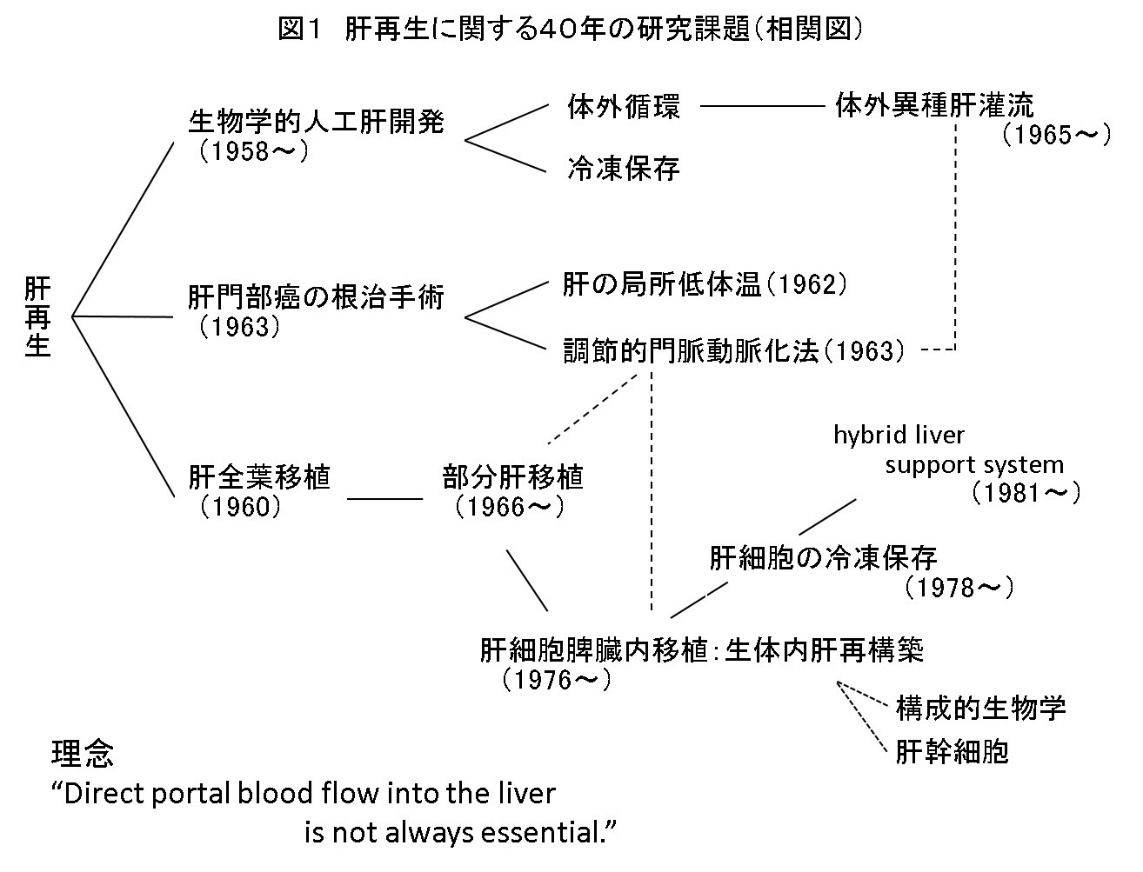
三上教授から与えられた具体的な(?)課題は、「切除限界の対応策を」検討するように命ぜられ、残存肝臓が再生するまでの間の機能補助を人工的に行う肝臓装置の開発と、死体からの提供を期待しての肝臓移植をテーマにと即断し、置換(再建)外科の研究に歩を進めた。
しかし、仲間も少なく、研究費もなく、暗夜に光なしで出されたに等しかった。幸い、製薬会社の課長の好意(同情?)で動物実験に使用する薬品の提供を受けることになった。さらに、世界で初めて人工肝臓なる装置を試作した 故堀 原一先生(後に筑波大副学長)との偶然の出会い、生涯の友(恩人)が装置の追試実験を許可し、その上、装置一式(血液駆動ポンプ、麻酔器など)を請求書無しで貸与してくれた機械屋社長のもとに共に出向いてくれた。
昼間の診療後、4、5人の院生グループは肝臓全摘出犬と2頭の正常犬との生セロハンチューブを介しての交差血液還流に犬の血に塗れながら、実験に精を出した。臨床で施行するには健常犬4頭を清潔領域で使用するなどの問題もあり、私共は2年後輩の 故能勢 之彦先生(後に、クリーブランド・クリニック人工臓器部門研究所長)のアイデアで、肝臓切片や凍結肝顆粒を生犬に変え、Reactorとして使用する所謂、生物学的人工肝臓を試作し、実験を繰り返した。しかし、代謝改善は3〜40分で、実用には至らず、徒労に帰したが、体外循環の手法や冷凍保存技術を習得し、その後の研究に役立った。
また、犬の肝臓全葉移植を助教授まで駆り出して試みたが、移植肝のoutflow blockや oozingによる出血などで術後24時間の生存を得られず失敗に終わったが、低体温法や無肝時の腸管系の血液鬱滞対応策などを消化器病学会大会で‘60年に公表した。
2.肝再生に門脈血の流入は不可欠なのか?;終生の研究理念の確立
1962年に次回の外科学会総会会長から三上教授に肝門癌外科治療についての特別講演の依頼があり、私共の肝臓研究班が下請けを担当することになった。癌の拡大切除に伴い、その後に肝門部に出入する肝管、門脈、動脈の再建をしなければならない。
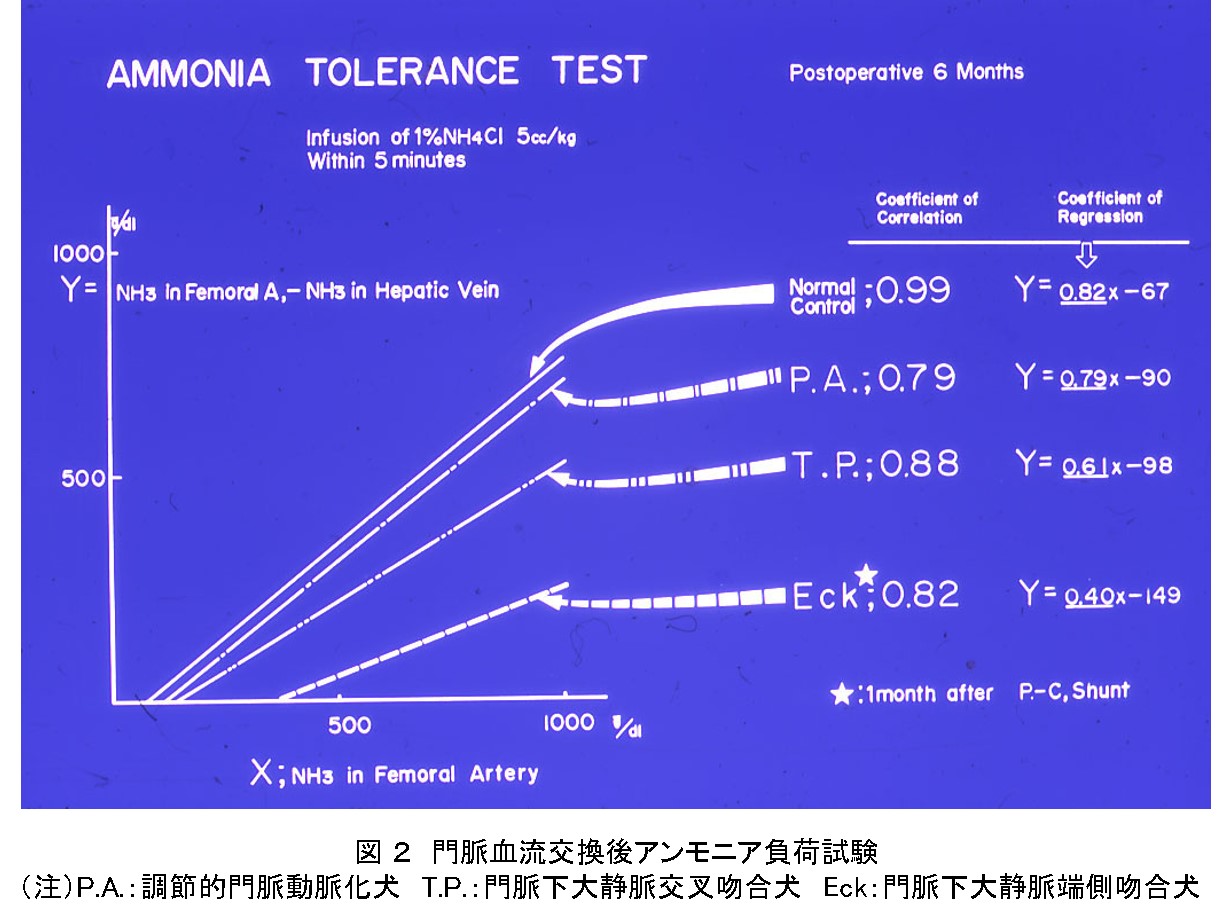
当時はまだmicrovascular techniqueによる動脈再建は至難の業で、その解決策として調節的門脈動脈化法を考案し犬の実験を重ね、施行犬の術後6か月のアンモニア解毒能力は有意差なく(図2)、1年半後の組織像もほぼ正常であった。本法の要点は動脈と肝側門脈間のグラフトの一部に狭窄を設けることで拍動流を定常流に変え、また流入量を調節することである。その結果、肝臓は約80%の動脈血の流入のみでも形態と機能を長期にわたり維持できることを確認した。
また、脈管再建時の肝虚血の対応策として、以前に経験した体外循環による肝局所低体温法を開発し、これによって肝温25〜26℃では90分間の虚血に堪えた。この門脈動脈化法の成果は「肝臓は二重血行支配であり、肝再生には門脈因子の重要性」が定説化していたのに反し、私の理念は「Direct portal blood flow into the liver is not always essential.」と変わり、その後の部分肝移植や脾臓内肝細胞移植へと進展した。
3.肝再生力の利用で部分肝移植への挑戦;英語音痴の日本人の奮戦記
1964年9月、堀先生の後釜として、ハーバード大学外科のresearch fellowとなった。Chairmanである肝臓外科で著名な故McDermott教授に研究計画の提出をしたところ、英語音痴の私が英国人や米国人とチームを作れるか、かつ、死体肝の入手が容易な状況での部分肝移植の研究は拒否され、門脈下大静脈吻合の問題点検討を命じられた。
動物実験室は病院の手術室並み、縫合糸やゴム手袋もディスポーザブル、当時の日本の状況とは天と地の相違、加えて潤沢な研究費に目を見張った。与えられた課題もS.G.O.なる外科の専門誌に掲載が決まり他に2、3の論文も仕上げた。
2年目にBossから部分肝移植実験の許可がおりた。英語音痴の私であったが、メスを持つと、犬の門脈下大静脈端側吻合を10分以内で手早く行う外科医の能力を認められ、Fellow仲間も協力してくれることになった。総胆管結紮による黄胆犬に正常犬の肝左葉を腹腔内に移植した。移植肝の血行再建は調整的門脈動脈化により動脈血のみが供給された。移植肝からの胆汁の排出によって宿主は減黄された。また、移植肝には再生像が確認されたことから、部分肝移植は手技上可能であり、この方法によって、提供者の肝臓は再生により復元し、患者に移植された部分肝も宿主の成長に伴い再生、肥大する可能性を示唆した。この成果は帰国後にAnnals of Surgeryに掲載されて、世界で初めての報告と鼻を高くしたが、同じような着想は同時代に数人はいるもので‘60年代には相前後して報告された。
帰国後に、部分肝移植の同所性移植の実験を続行したが、大学学園紛争の勃発で中断せざるを得なかった。多くの基礎実験の成功は必ずしも臨床応用にそのままで繋がるものではなく、問題点を解決しながら、再生力を利用した部分肝移植の臨床例の実現には約20年後の‘84年まで待たなければならなかった。
4.新設医科大学旭川医大への転任;外科医の研究がマクロからミクロの世界へ
全国で医大建設ブームが起り、国は1県1医科大学設置を計画し、一期校として、北海道の旭川と本州の2校が決まった。学年進行で教授が発令されたので、私は開学3年目の1975年4月に外科学第二講座の教授として赴任した。しかし、建設予定地には研究棟も病院もなく、市立病院の病室2室を仮住まいとして与えられた。正に陸に上がった河童も同然であった。
1)脾臓内肝細胞移植の着想は暇の効用か?
成すこともなく札幌での講演会に出向いた。講演内容は遊離したβ細胞の移植で、薬物性糖尿病ラットの治療実験であった。スライドを眺めながら私の網膜にはβ細胞がいつの間にか肝細胞に代わっていた。「肝硬変は働き手の肝細胞が結合組織で雁字搦めに閉じ込められて機能を十分に発揮出来ない。それならば縄(結合織)を解けば自由になった肝細胞はその類まれな再生力で組織塊となり、機能を発揮するのでは? 遊離肝細胞の移植部位は肝硬変症では腫大し、容量を増し、かつ血液豊富な脾臓なら・・・」とのアイデアが単純な私の脳裏を駆け巡った。
新しい研究棟が出来るまで、海外の友人達の下に留学していた仲間が戻り、再び、僅かな講座費からラットを購入、マクロの外科医が細胞分離などミクロの世界へと、机と椅子以外には殆ど無に近い状況下での出発であった。
2)移植遊離肝細胞の脾臓内増殖過程;幸運が重なり合って
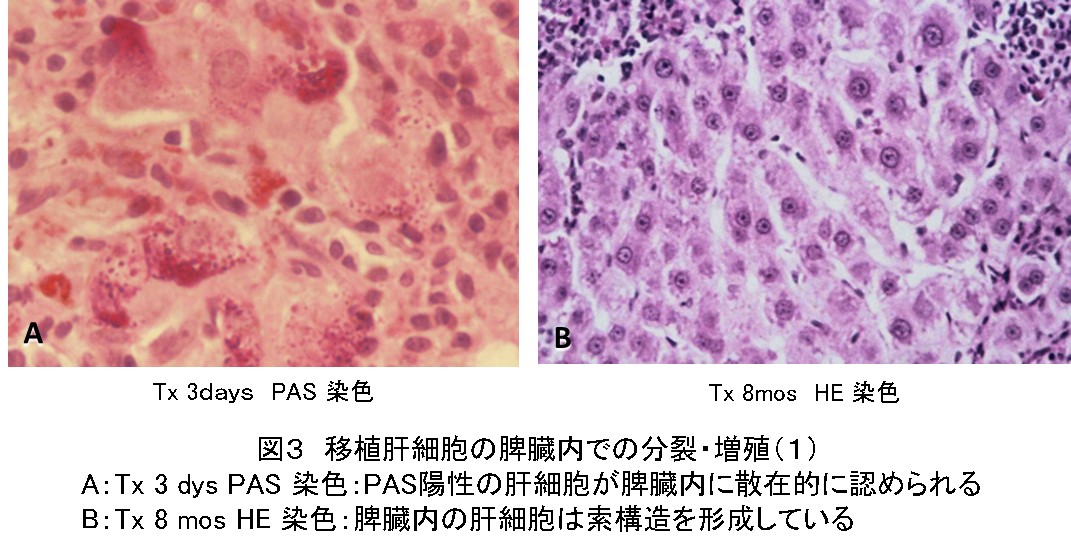
約20匹前後の同系ラットに一個の肝臓から遊離した肝細胞、106個を脾臓内に注入移植した。移植後3日目の脾臓組織にPAS染織に染まる赤紫色の顆粒が輝く肝細胞を認めた。異所で3日間、生存した数個の肝細胞はその増殖力で増えるだろうとの考えで飼育し続けた。たまたま、移植8か月後の3匹のラットを犠牲死させた脾臓の組織像は赤脾髄内に増殖し、かつ分化した肝細胞索を形成していた。研究の定石である術後2、4週、3、6か月と検索を行なわなかったのは、研究費の欠乏であり、また手技上単純なことであるが、移植時に脾静脈を遮断、注射針の刺入部の結紮操作を行ったこと、後に追加実験で分かったことであるが、移植細胞数が至適であったなどの偶然の重なりが期待以上の成果を産んだ。
この成果は‘76年秋、日本移植学会の一般演題で採用された。世界初の仕事であったが、座長のコメントは数個の肝細胞の残存はどれだけの意味があるか?と手厳しかった。しかし、米国帰りの一外科医が称賛してくれた。また、‘78年春、ヘルシンキで開催された第13回ヨーロッパ研究外科学会で発表した。質疑になると、ミネソタ大学とカロリンスカ研究所の二人が私と同じアイデアで実験を行ったが失敗に終わったと、成功の理由は?と問われた。彼らが定石どおり、経日的組織観察で移植細胞が激減し、その後に残留細胞が増殖するのを待たずに実験を中止したことによった。降壇しようとした時、万雷の賞賛の拍手が起こり、また、コロラド大学のEiseman教授が立ち上がり「この脾臓をHepatized Spleen、(肝化脾)と呼称しよう」と提案してくれた。
爾来、脾臓内肝細胞移植が私の教室の主研究テーマとして多くの課題に取り組んだ(表1)(図3)。

3)肝細胞脾臓内移植のラット実験の成果;自然の摂理を見る
同系ラットの肝細胞を脾臓内に5×106個注入移植すると、直後の残存率は10〜15%と少ない。残生した肝細胞は2〜3カ月後から分裂、増殖をし始める。1年前後には肉眼的に識別できる肝組織が構築される(図4)。
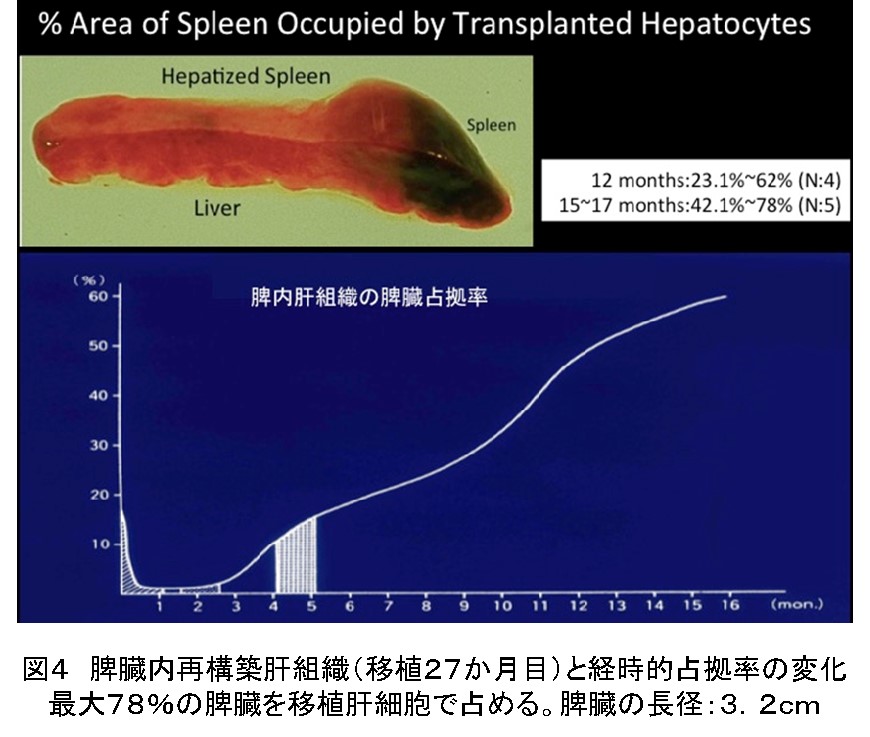
その過程で肝細胞索はヤツメウナギから両生類さらには哺乳類と進化の過程をとる(図5)。
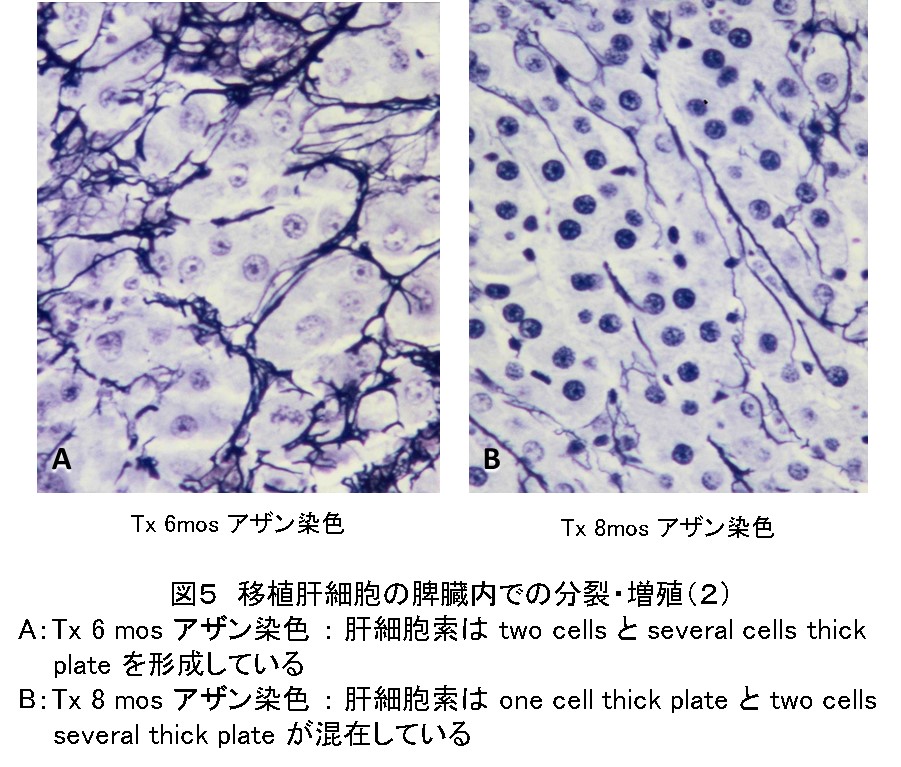
また、移植18か月後のHE染織像では白脾髄を除き赤脾髄は再構築された再構築肝組織で埋め尽くされた(図6)。
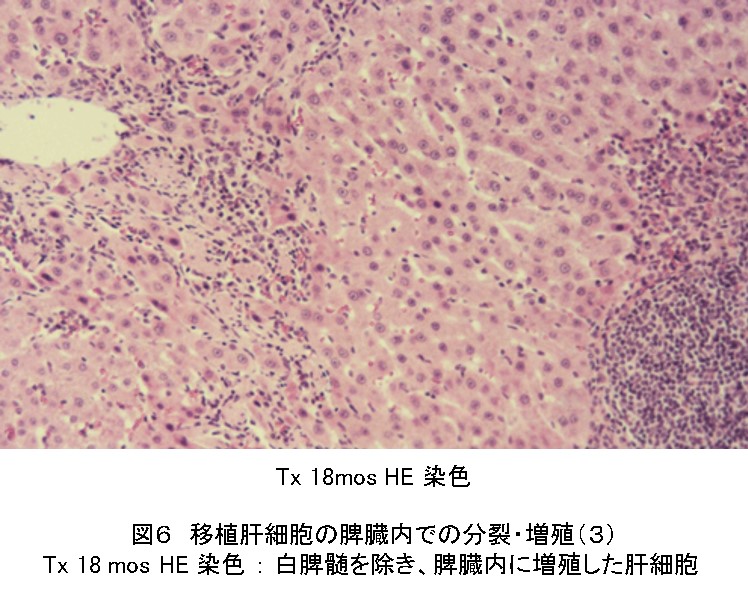
また、電顕像で特徴的な形態と機能を有する肝臓の類洞構造が認められた(図7)。
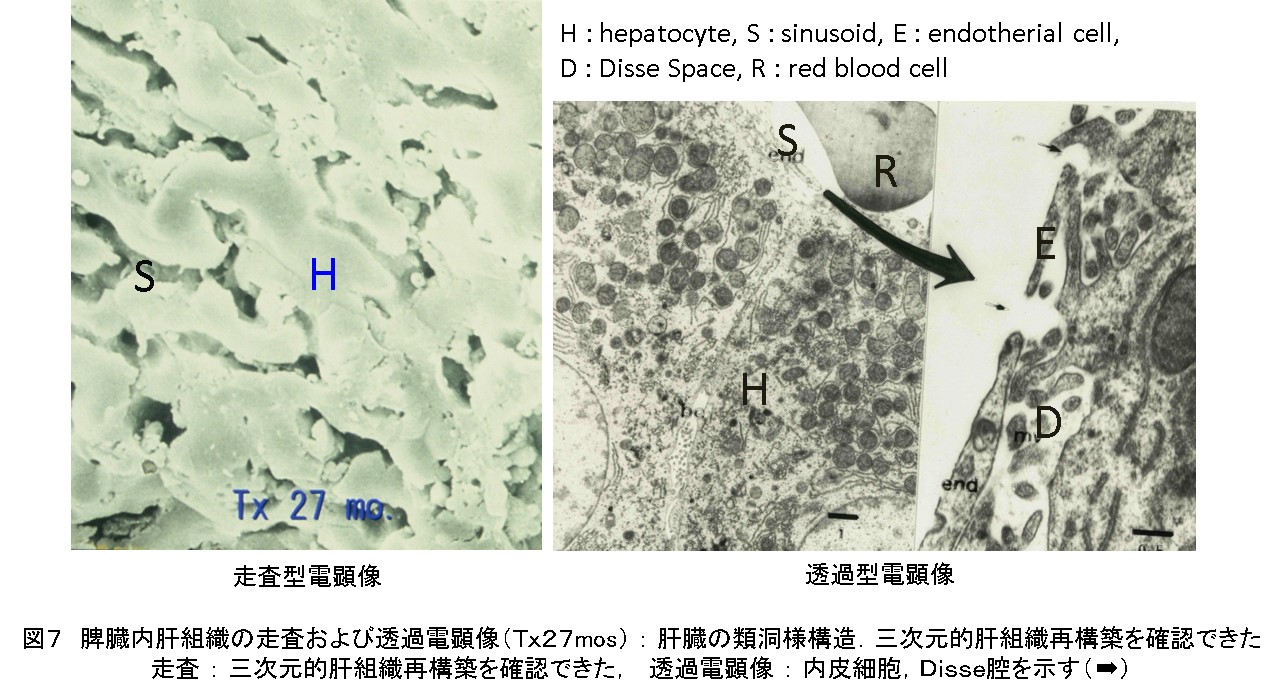
このように脾臓内に移植された肝細胞は、肝に特有な類洞構造をもつ三次元的組織再構築を行うことを確認した報告は世界で初めてであった。また、肝化脾の機能をアンモニア負荷試験や無アルブミンラット、その他の諸検査で検索した。
特に無アルブミンラットに同系ラット肝細胞脾臓移植を行うと、肝細胞増殖に伴い血清アルブミン値は増加し、移植18か月後には最大122mg/dlに達し、肝化脾を摘出すると血清アルブミン値は急激に低下することから、アルブミンの産生は脾臓内の肝組織によることを証明しえた(図8)。
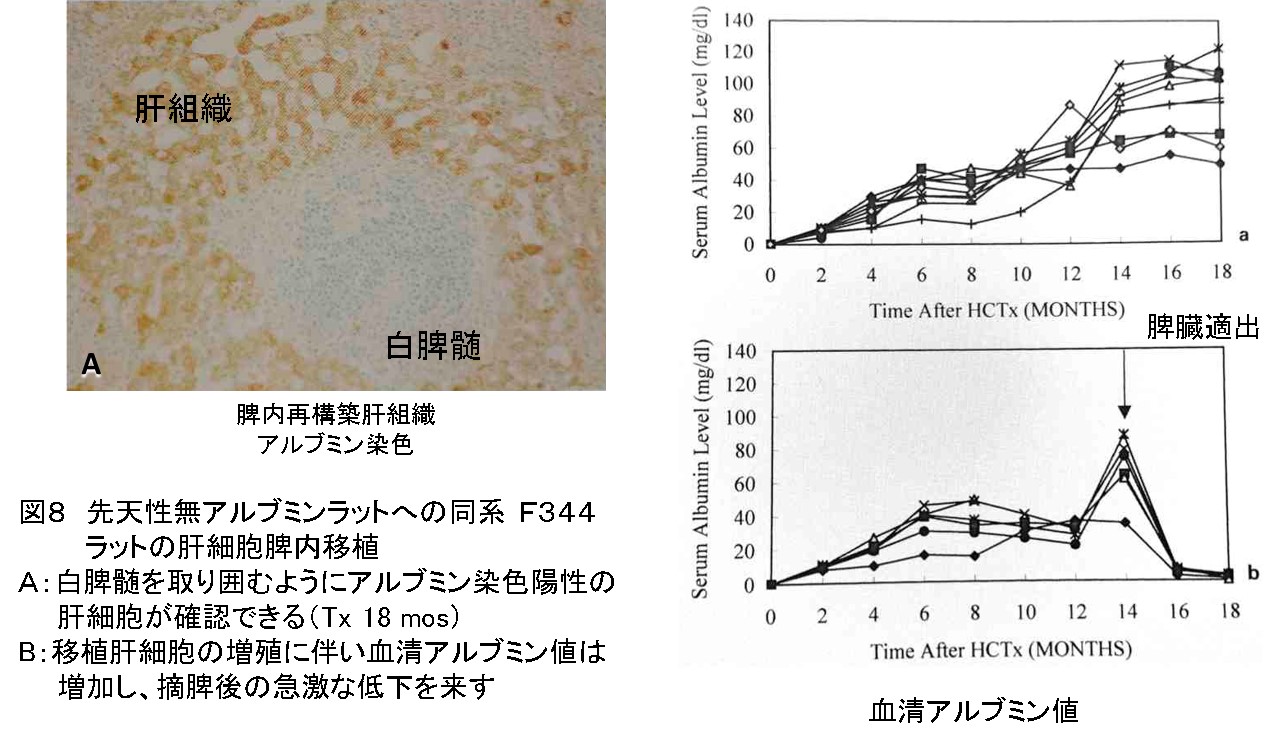
また、分離肝細胞を冷凍保存した後、解凍したところ、精子や卵子の保存と同じくviableであることも確認した。脾臓内移植後にも肝臓組織の再構築を果した。
4)ラットの実験で浮上した問題点、課題
a)なぜ脾臓の肝臓化に長い日時を要するのか?
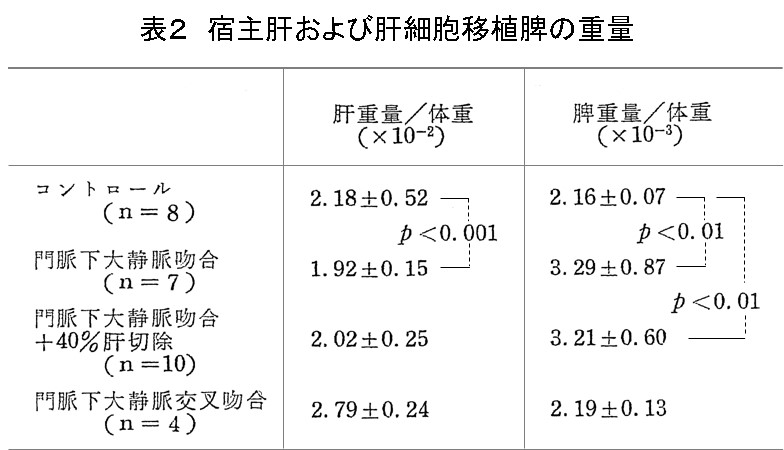
脾臓の1/2〜2/3を占める再構築肝臓が形成されるに約1年を要した。また、肝化脾の重量は最大1gで、この重量は宿主肝臓と肝化脾の合計重量の体重比内であった。移植を受けたラットの生存中は、移植肝細胞は悪性化しなかったので理解できる。宿主肝切除などの種々の肝再生を刺激する実験では一時的に肥大効果を認めたが、宿主肝臓の再生後は元の大きさに復した。ただし、門脈下大静脈端側吻合(Eck)(肝臓の萎縮と慢性肝機能不全となる)を施行した肝化脾は重量が倍加したが、門脈下大静脈交差吻合(PCT)を施したラットの肝化脾での重量増加はなかった。したがって、移植時に門脈下大静脈吻合(PCS)したラットに施行したならば組織再構築過程は早まる可能性はある。
b)生体内の二つの肝臓間の競合現象について
上記の結果で問題になったのがPCS群で再生の門脈因子の重要性を改めて知ったのではないかと。しかし、PCS群と同じく宿主肝をバイパスして門脈因子が肝化脾に流入するPCT群では、肝化脾や宿主肝の重量はコントロール群と有意差がなく、両群の差はPCS群の宿主肝の萎縮による代償性肥大によると考えられる(表2)(図9)。
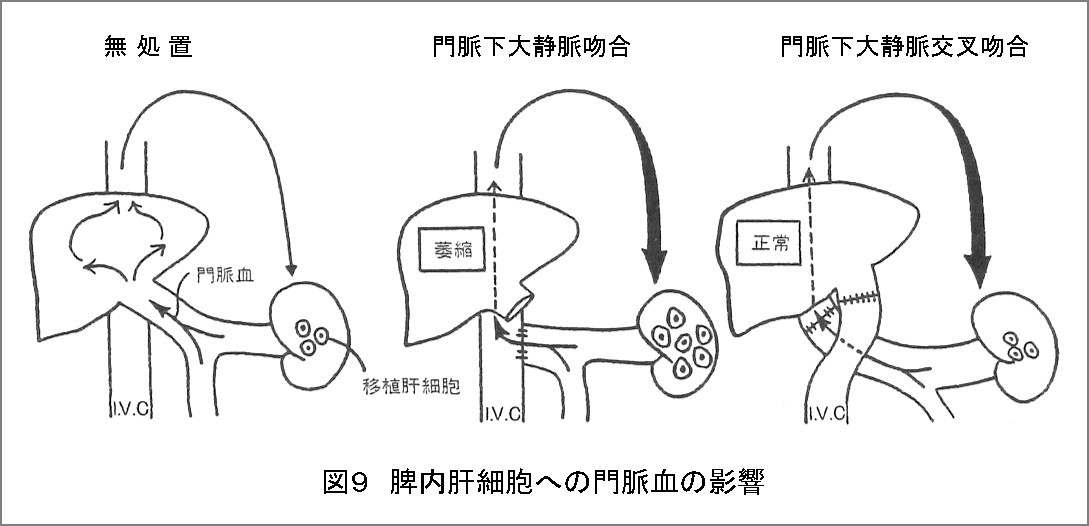
また、共同研究を行っていたHanover大学のDr. Lösgenは肝細胞のcytochromeやmitochondriaの酵素を測定し、宿主肝の機能低下するPCS群のみ肝化脾は正常肝と同じ値を示し、コントロール群とPCT群は正常脾臓の酵素値であったと非常に興味ある研究成果を報告した(表3)。
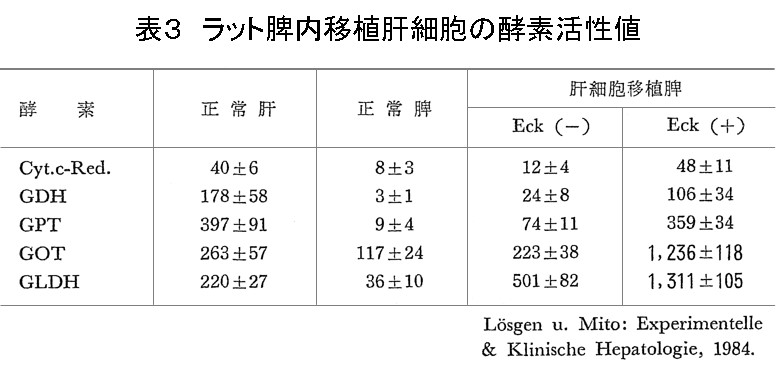
宿主肝と補助肝との競合現象はヒトの肝移植で病肝を腹腔内に温存し、補助肝臓を移植するauxiliary transplantationでもみられ、病肝の悪化で補助肝の機能が増大する。また、先天性にある異所性肝臓は機能低下した肝硬変症で発見されることが多い。いずれにしても、競合現象の更なる追求が必要である。
c)庇を貸して母屋を取った肝化脾の類洞形成
移植肝細胞は脾臓のビルロート腔にある脾洞の外側に生着し、分裂増殖する過程で脾洞を取り込んだ形で類洞化が見られる。篩板(fenestration)がない脾洞の内皮細胞とは異なり、肝化脾類洞内皮細胞には篩板が存在する。当時は、正常肝類洞内皮細胞のマーキング法が確立されておらず脾洞の内皮細胞が形態変化したのか、移植時のcontaminationであるかの確認は今後の検討課題である。また、肝化脾類洞壁に存在しているKupffer細胞や肝星細胞のoriginについても今後の検索が待たれる。
d)肝化脾の胆汁分泌はどの様になっているか?
移植肝細胞のbiliary surfaceにはアルカリホスファターゼに染まる毛細胆管が認められるが、その後の胆汁排出路の胆管は形成されない。胆道系細胞を移植していないので当然のことではあるが、胆汁分泌のtracerであるhorseradish peroxidase (HRP)を用いて検索すると、HRPの粒子が毛細胆管に排出していることが確認された(図10、11)。すなわち、移植肝細胞にも胆汁排出の機能があることが示唆された。
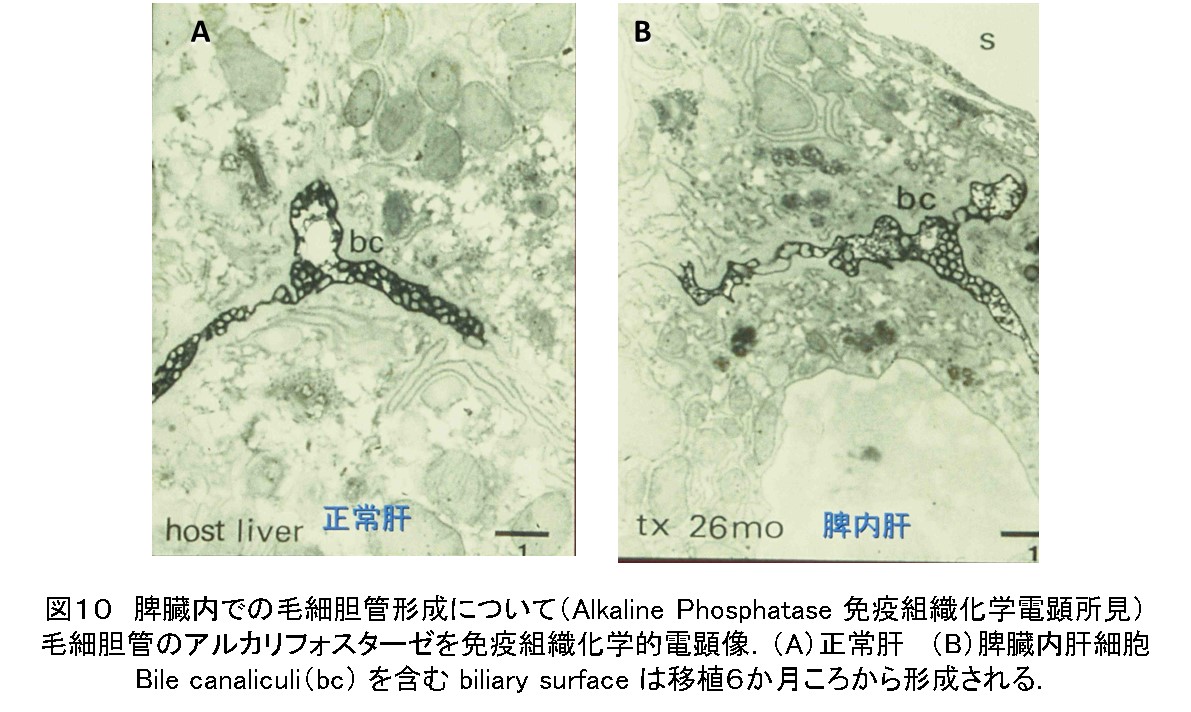
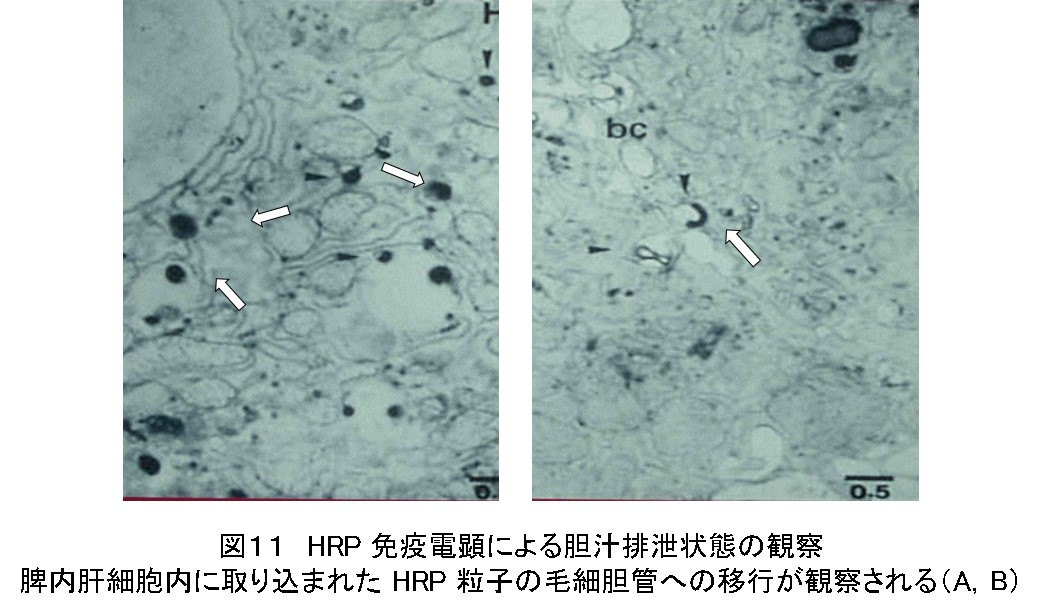
学会などでの発表後には胆汁排泄はどうなるかの質問が多かった。数え切れないほどの再構築肝の組織を観察したが、胆汁栓を認めた事がない。血管内への排出を推測しているが確証は無い。
肝臓病理学の泰斗、Grisham, J.W. 教授が、20世紀初頭からの肝臓の組織や部分肝の異所性移植の文献をレビューし、加えて、ご自身の実験結果を発表しているが、ラットの部分肝の異所性移植後1年の観察で正常形態と機能の維持に門脈血の流入は不要で動脈血の供給と胆汁排出の重要性を説かれている。
私共の肝化脾も胆汁排出に関して検索が重要課題であるが、先天性肝外無胆道症に施行されたSterling, J.A.の手技(多数の細いプラスチック管を肝に挿入し胆汁排泄を促す)は一つの解決策かもしれない。
e)同系ラットの胎児肝組織脾臓内移植;果たして肝臓を形成するのか?
肝細胞脾臓内移植を2年半にわたる観察で哺乳類の肝細胞索の大きな集団が再構築され機能を発揮したが、本来の肝臓が有する小葉構造や胆管形成は認められなかった。胎生期の肝臓の主な機能は造血であるが出生後はその機能を漸減し、取って代り肝細胞が機能を発揮する。そこで、胎仔肝組織を生体内の培養器のような脾臓に移植し、経過を観察した。胎生18〜19日目の胎仔肝臓を細断し移植すると、移植4週後は予期に反し、増殖した肝細胞集団とその周りに個別に増殖した個々の胆管細胞が観察された。その所見は1年後もほぼ同じで、肝細胞群の減少に比し著明な胆管細胞が個々に増殖していた。これらは所期の期待に反するものであった。
この研究過程で過去の文献検索を行い、約20年前の‘63年にマウスで同じ研究がすでに行われていたこと知り、驚き、ここでも「温故知新」の大切さを痛感した。
iPS細胞から誘導したLiver bud(肝芽と称している)を大網内に移植し、肝芽内の血管と移植部位からの脈管が吻合したので3次元の肝臓を作製したと2013年に公表され大いに期待したが、その後に肝芽が肝臓に成長したとの報告はない。この論文の共同著者の教授は私に慢性実験は中止したと告げられた。膨大な研究費をつぎ込んで、今や最先端の再生医学と期待されているES細胞やiPS細胞をもとに3次元の臓器作製報告は寡聞にして私は知らない。
5.イヌとサルの肝細胞脾臓内移植の実験;果して、臨床に応用できるのか?
臨床応用するために中動物のイヌの自家移植実験を試みた。5.6x106個を脾臓内に移植した。1か月後に移植肝細胞は残生していたが、3か月後には増殖することなく、数を減じ、1年後には移植肝細胞は消滅した。ラットでの成功体験を即座に変えることが出来ずに2年を浪費してしまった。宿主肝が部分切除後の再生が終わると異所性肝臓は不要なのか、また、循環動態で絶えず大きさを変化させるイヌの脾臓の構造と機能検索を怠った事によると考えた。
最後の望みを託してサルの自家肝細胞脾臓内移植を試みた。2.7x106個を移植し、1年後に移植肝細胞の増殖を促すため、宿主に門脈下大静脈端側吻合を施行した。その3か月後の脾臓内にはラットと同じく肝細胞索と類洞構造が明確な肝細胞集団が結節状に認められた(図12)。霊長類のサルの実験は臨床応用の可能性を示唆するものであった。
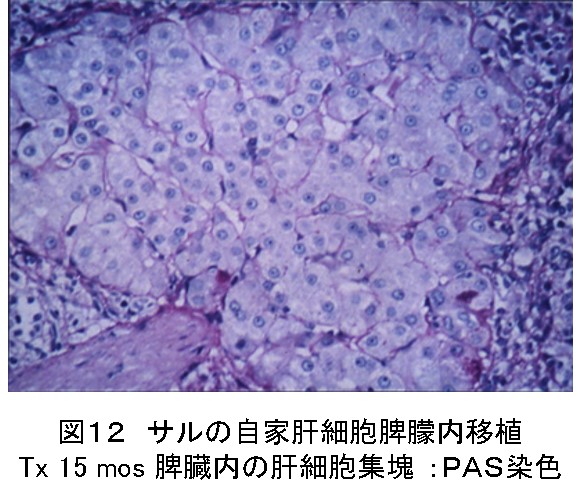
イヌとサルの実験で肝細胞分離過程がコラゲナーゼの濃度など動物種によって異なることを学んだ。また、イヌの宿主に予め門脈下大静脈吻合を施行した後に脾内肝細胞移植を行った場合など更なる課題は残った。
6.臨床例での試験治療
サルの実験結果がTVや新聞で報道されると、自己の肝細胞移植を希望する多くの患者さんが来院するようになった。胆石症や食道静脈瘤で手術の適応のある方に開腹時に試験的に試みることを了解していただき6症例に施行した。肝左葉の一部(約40g)を独自に開発した分離装置で肝細胞を分離し、症例により異なるが107~8個を脾内に注入移植した。移植後は脾臓内の肝細胞を99m Tc-PMTのシンチグラフィーで追跡した。術後1か月と3か月目に移植細胞残留を思わせる所見を得たが、1年後には全ての症例で消失した。期待した成果は得られず、何故、ヒト肝細胞は脾臓内で増殖しないかの原因を追求しなければならない。動物種による差の解明は「脾臓の謎」といわれる機能と構造を学ぶことで道が開けるかもしれない。また、私は大学なる研究の場を去る時、この分野の研究者の方々へ纏めた資料の提供などに資すればと斯界の専門家の方々の協力で、単行本、「Hepatocyte Transplantation」を出版することができた。
7.終わりにあたって
1970年後半から2000年代当初までは臓器構成細胞の分離、移植によって機能不全の治療や幹細胞の存在や分化、更には可塑性などの研究が医学分野では所謂、トレンドであった。しかし、今日ではES細胞やiPS細胞の出現で、これを利用した再生医学が斯界の花となり、胎児や成人臓器構成細胞の分離や分化の研究はやや昔物語となりつつある。
期待されるES細胞やiPS細胞が我々臨床家のベッドサイドで使用されるには、なお、多くの基礎実験の成果の積み重ねが必須であり、恐らく一般に普及するには約20年は要するのでないかと思われる。
肝細胞の研究に携わっている若き方々が一時、立ち止まり、過去の同じ分野の先輩たちの業績を振り返ってみると、ご自分の計画の修正や次の歩を進める糧となる事もある。
一外科医の私の40年に亘る諸々の研究成果が何時か何処かで、一粒の種となり、成長することを夢見ているが、私が書き述べた数々の成果は研究仲間の独自の発想と努力の賜物であり、深甚の感謝の意を表し、終わりにしたい。
※なお、図3〜8、10〜12および表1は、著者の論文からの転載許可を日本門脈圧亢進症学会から得たものである。
各項目の主な参考文献
1.肝臓外科との出会い
- 三上二郎:肝広汎切除. 日外誌, 57;898, S31
- Gans H: Introduction of Hepatic Surgery, Elesvier, New York,1955.
- 堀 原一:人口肝臓. 現代外科学大系 中山書店 25;115, 1969.
- 三上二郎,葛西洋一,薘見恒生,水戸廸郎,ほか:人口肝臓-特に体外代謝について-. 総合医学 17;538, 1960.
- 水戸廸郎,西村昭男,住吉 章,能勢之彦ほか:模型人工門臓(肝・腎)の体外循環について.総合医学 17;538,1960.
- G. Brunner, M. Mito, Eds., Artificial liver support:concepts, methods, results.Springer-Verlag,1992.
- 山田淳一,ほか:肝全剔後同種肝移植の研究(第一報)日消器会誌 57;1581, 1960.
2.肝再生に門脈血は不可欠か?
- 三上二郎:肝癌に対する拡大手術の検討-肝門部癌の外科治療-日外会誌 65;1040, S31.
- 三上二郎,水戸廸郎:肝門部癌の診断法と根治手術術式 臨床外科 19;1441, S39.
- Mito. M., Tamaki. A., Kon. T., Ohira. S., & Mikami. J.:Experimental studies on differential hypothermia of the liver. J. Surg. Research, 5;207,1965.
門脈因子については4.の4)のb)生体内の2つの肝臓の競合現象の項でもあげている
3.肝再生力の利用で部分肝移植への挑戦
- 水戸廸郎著,沈黙の臓器と語る. NHKブックスNo.743, 1995.
- Mito. M., Pikula. J. V., Mcdermott. W. V. Jr.: The effect of portacaval transposition on renal and adrenal function. S. G. O. 123;1289,1966.
- Van der Heyde MN. et al: Survival of hepatectomized dogs with partial liver transplants. Surg. 59;1079,1966.
- Mito. M. et al: Partial heterotopic liver homograft in dogs utilizing portal arterialization. Ann Surg 165;20,1967.
- 水戸廸郎,山本 哲,澤 雅之:肝部分移植の実験研究から臨床応用までの歩み,今日の移植,4;111,1991.
- Bismuth H, Houssin D: Reduced-sized orthotopic liver graft in hepatic transplantation in children. Surgery 95,367,1984.
- Sigel B, et al: Studies of liver lobes auto-transplanted outside the abdominal cavity. S. G. O. 124;5251967.
- Aoki H, et al: Partial liver transplantation with primary revascularization in dogs. Preliminary report on new method and its theoretical background. Keio J. Med. 16;205,1967.
- Grisham, J. W., Leong, G. F., Hole, B.V.; Heterotopic partial autotransplantation of rat liver: Technic and demonstration of structure and function of the graft. Cancer Research 24;1474,1964.
- 水戸廸郎,招待講演,肝臓機能再建を志した-外科医の足跡-人工肝・部分肝・肝細胞移植をめぐって-. 日小外会誌 28;253,1992.
4.新設医科大学旭川医大への転任
4の2)移植遊離細胞の肝臓内増殖過程
- 江端英隆,大西俊郎,大野正博,草野滿夫,関口定美,水戸廸郎:ラット肝細胞移植の実験的研究(第一報).移植(総会臨時号),11;83,1976.
- 水戸廸郎,江端英隆,草野滿夫,大西俊郎:脾臓内肝細胞移植. 醫學のあゆみ,111;362, 1979.
- Mito M., et al: Morphology and function of isolated hepatocytes transplanted into rat spleen. Transplantation, 28;499,1979.
- 水戸廸郎,江端英隆:肝細胞脾内移植法による肝細胞増殖機構の解明および肝機能補助の基礎的研究.日本医師会雑誌, 83;545, 1980.
- 水戸廸郎:生体内培養モデルでみた肝細胞の分化.消化器の発生と分化,藤田哲也・川井啓一編,大阪書籍,大阪, 111, 1988.
- Ikebukuro H, Inagaki M, Mito M, et al: Prolonged function of hepatocytes transplanted into the spleens of Nagase analbuminemic rats. Eur Surg Res, 31;39,1999.
- 水戸廸郎,草野滿夫:長期冷凍保存肝細胞の脾内移植.外科治療,51;126, 1984.
- 葛西眞一,水戸廸郎. 組織冷凍保存技術の進歩.病態生理,6;413, 1987.
4の4)ラット実験で浮上した問題点・課題
a)およびb)競合現象
- 水戸廸郎:肝細胞移植が提起する諸問題(第85回日本外科学会会長推薦講演),日本外科学会雑誌, 9;993, 1985.
- 水戸廸郎:脾内肝細胞移植の臨床への道程.肝増学の進歩,肝臓研究会,12;12,1986.
- Mito M., Kusano M., Sawa M., et al: Hepatocyte transplantation for hepatic failure. Transplantation Reviews, 7;35, 1993.
- 水戸廸郎,江端英隆,草野滿夫:門脈血流と肝再生. 肝胆膵, 283, 1981.
- Fortner, JG., Kinne, DW., Shiu, MH., et al: Clinical liver heterotopic (auxiliary) transplantation. Surgery, 74;739,1973.
- Houssin D., Franco D., Berthelet P., Bismuth H.: Heterotopic liver transplantation in end-stage HBsAg-positive cirrhosis. Lancet, 990 May 10;1980.
c)、d)類洞形成と胆汁分泌
- Kusano M., Mito M.:Observations on the fine structure of long-survived isolated hepatocytes inoculated into rat spleen. Gastroenterology 82;616,1982
- Sterling J.A.:Long-term survival of infants without extrahepatic bile ducts. Am J Surg, 112:382, 1966
e)胎児肝組織の移植
- Ebata H., Mito M., et al: Intrasplenic fetal rat hepatic tissue isotransplantation. Transplantation, 39;77, 1985
- 中村康司,宮島 篤:胎生肝の分化,肝胆膵 42;167, 2001.
- Takebe T., Taniguchi H., et al: Vascularized and functional human liver from an iPSC-derived organ bud transplant. Nature,499, 2013.
5.イヌとサルの肝細胞移植,6)臨床例
- Kasai S, Sawa M, Kondoh K, et al: Intransplenic hepatocyte transplantation in mammal. Transplantation Proceeding. 19;992,1987.
- Mito M., Kusano M., et al:Hepatocyte transplantation in man. Cell Transplantation,2;65,1993.
- Gupta S, Chowdhary JR:Hepatocyte transplantation: back to the future. Hepatology, 15;156,1992.
- Ohashi K., Park F., Sc. Kay M.A., et al:Hepatocyte transplantation: clinical and experimental application. Journal of Molecular Medicine 79;617,2001.
- Allen KJ, Soriano HE:Liver cell transplantation: The road to clinical application. Journal of Laboratory and Clinical Medicine, 138:298, 2001.
- Fisher RA, Strom SC:Human hepatocyte transplantation: worldwide results. Transplantation,82:441,2006.
- 水戸廸郎,草野滿夫,脾内肝細胞移植:どのようにして正常な肝細胞が脾臓に生着し、増殖したのか?,日本門脈圧亢進症,22;119, 2016.
- Mito M., Sawa M.,et al:Hepatocyte Transplantation: Karger Landes Systems, Basel-Freiburg, Tokyo. 1997.










