研究交流
肝細胞移植―レシピエントに対する前処置は必要か―
国立成育医療研究センター 研究所 再生医療センター
絵野沢 伸
はじめに
COVID-19の影響でオンライン開催となった第27回肝細胞研究会(水口裕之会長、2020年12月)のシンポジウム「肝臓を使い、肝臓を操る」(オーガナイザー/座長;石田誠一教授・後藤昌史教授)にて「肝の細胞治療―基礎から臨床へ」と題し、国立成育医療研究センターで行われた臨床肝細胞移植を紹介する機会をいただきました。オンライン講演は不慣れでしたが水口会長と事務局のきめ細かいご配慮ご指導により、安心して発表に臨むことができました。本稿では講演の補遺の意味を込め、マウスを用いた基礎研究(Cui et al(1))をモチーフとして、臨床肝細胞移植における前処置のあり方について私見を述べたいと思います。
造血幹細胞移植に見る前処置の変遷
造血幹細胞移植では前処置として薬剤や放射線による骨髄の抑え込み(骨髄抑制)が行われ、長らく"移植細胞の場を設ける"という意義づけがなされてきた。造血幹細胞移植は放射線被曝の治療として始まり、それが血液腫瘍治療の骨髄抑制と結びついた経緯を考えると、この組み合わせの必然性はうなずける。しかしながら、最近は移植細胞の生着に必ずしも徹底的な骨髄抑制は不要との考えに変わってきたという(2)。もちろん同種移植の場合は拒絶反応に対する免疫抑制が必要だが、骨髄抑制ほど侵襲性が強いものではない。こうして非腫瘍性の血液疾患―再生不良性貧血や免疫不全症、あるいは先天代謝異常であるムコ多糖症などに対しても造血幹細胞移植が行われるようになってきた。
肝細胞移植における前処置
動物実験では移植前に外因性もしくは内因性の様々な肝障害を与えている(やや古いが総説(3)のTable 1によくまとめられている)。部分肝切除、放射線照射、肝毒性薬物投与、uPA-transgenicマウスの利用、ganciclovir 応答性thymidine kinase遺伝子導入によるconditional肝障害などである。最近の成果として、立野らはuPA/Scidマウス肝にヒトの先天代謝異常であるornithine transcarbamylase欠損症由来初代肝細胞を移植し80%以上の細胞置換を達成、病態の再現に成功した(4)。この系により、遺伝子治療などの基礎実験や、希少なヒト病態肝細胞を新鮮細胞として得て培養実験に供し得るようになった。ただ、動物実験の目的は肝細胞移植の治療スキームとはややずれており、こういった侵襲性介入をそのまま臨床プロトコールに持ち込むことはできない。
臨床研究プロトコールのロジック構築
国立成育医療研究センターで臨床肝細胞移植プロジェクトの検討を開始した2008年当時、海外における肝細胞移植は先天代謝異常肝疾患 21症例、慢性肝不全 20症例、急性肝不全 37症例に試みられていた(5)。我々は標的疾患候補として、胆汁鬱滞性疾患(胆道閉鎖症に代表される)、先天代謝異常、劇症肝炎を検討し、先天代謝異常の一つ、尿素回路異常症を対象とすることにした。この決定は臨床側のリーダー笠原群生臓器移植センター長の考えによるところが大きい。当センターの肝細胞移植は、"重症高アンモニア血症を生じる先天代謝異常児で、即時的な肝移植ができない場合"を対象とし、肝移植が可能となるまでの"内科的治療を補助する"ことを目的に定めた。その頃から世界的にも小児先天代謝異常を標的とした肝細胞移植の報告が増加している。先天代謝異常肝は脂肪肝やグリコーゲン蓄積などの固有の病理所見を示す場合はあるものの炎症や壊死はみられない。そこに前処置を施すことなく、第三者から分離し凍結保存しておいたABO血液型一致または適合の同種肝細胞を門脈左枝経由で肝左葉外側区域に移植した(6)。その後、2019年に行ったヒト胚性幹(ES)細胞由来肝細胞移植も同じプロトコールによった。細胞移植後の臨床経過は安定し、高アンモニア血症で最も忌避すべき不可逆的中枢神経障害の発症はなく、5ヶ月齢時に生体部分肝移植を受け、その後も順調に生育している。このプロトコールが倫理審査で承認された最大の根拠は、他の治療を妨げるものではないという点であった。すなわち肝細胞移植以外の介入は、細胞移植後の免疫抑制剤投与(肝移植時の半量程度)を除き、行っていない。
レシピエントに対する前処置は必要か
臨床肝細胞移植においてもレシピエントに対し動物実験で行われるような何らかの介入処置を行わなくては効果がなかろうとの考え方がある。しかしながら、私は次の2条件を満たせば移植肝細胞の生着・増殖は可能ではないかと考えている;1)レシピエント肝が増殖相にある。レシピエントが新生児から幼小児期であることがこれに当たる、2)移植細胞が増殖可能な状態にある。成熟肝細胞ばかりでなく肝幹細胞様細胞を含む細胞集団を移植に用いる。それを裏付ける事例として図1を示す。これは文献1に報告した研究の予備検討時の一データである。図の説明に実験の要点を包み隠さず記した。条件1)としては生後2日目のScidマウス新生仔に移植をしたこと、条件2)としては移植細胞を新生仔ブタから得ている、非実質細胞画分も含む、向増殖性precultureを行ったことが挙げられる。国立成育医療研究センターで行った臨床肝細胞移植では条件2)は満たせなかったが、その後のヒト胚性幹(ES)細胞由来肝細胞移植はこれを充足したのではないかと思う。一般にin vitroで分化させた多能性幹細胞由来細胞は幼若で初代細胞に比べ機能が低いが、in vivo環境で生きぬく力は宿主への前処置という補助を受けなくても周囲の終分化細胞に優るものと期待している。
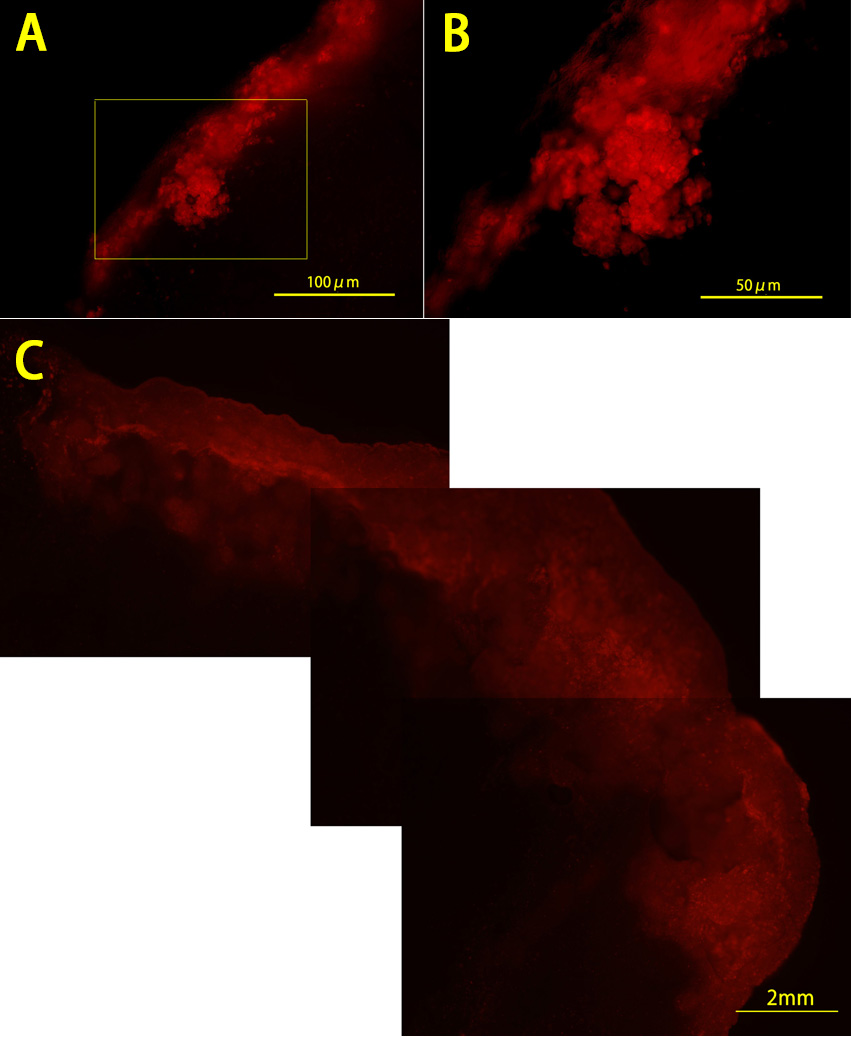
図1 Scidマウス肝内に生着したブタ肝細胞(移植後10週).移植した細胞はアルブミンプロモーター下で発現するクサビラオレンジ遺伝子導入ブタから分離・凍結保存した細胞で、解凍後3μmol/L myricetin存在下で24時間培養.CB17-Scidマウス新生仔(生後2日)の肝にマイクロシリンジを使い経皮的に直接注射した(2×10^5個/20μL/匹).肝組織にはfocalな増殖を思わせる肝細胞生着巣があり(A,B),肝全体に分布しているように見える(C).Scidマウスに前処置はしていない(抗asialo GM1抗体投与[NK細胞抑制]もしなかったが、これはした方がよかったかもしれない).移植細胞は生後1ヶ月以内の新生仔ブタから得たもので,低速遠心により実質細胞リッチにしただけの画分なので非実質細胞も含まれる.さらに移植前のmyricetin下の培養で増殖相へ誘導できたと考えられる.文献1の研究の予備検討の一例.
参考文献
- Cui C, Enosawa S, Matsunari H, Nagashima H, Umezawa A. Natural flavonol, myricetin, enhances the function and survival of cryopreserved hepatocytes in vitro and in vivo. Int J Mol Sci. 2019 Dec 4;20(24):6123. doi: 10.3390/ijms20246123. https://www.mdpi.com/1422-0067/20/24/6123
- 日本造血細胞移植学会.造血細胞移植ガイドライン ─ 移植前処置(第2版).2020年5月 https://www.jshct.com/uploads/files/guideline/02_01_zenshochi.pdf
- Guha C, Deb NJ, Sappal BS, Ghosh SS, Roy-Chowdhury N, Roy-Chowdhury J. Amplification of engrafted hepatocytes by preparative manipulation of the host liver. 2001 Jul;25(7):522-8. doi: 10.1046/j.1525-1594.2001.025007522.x.
- Sugahara G, Yamasaki C, Yanagi A, Furukawa S, Ogawa Y, Fukuda A, Enosawa S, Umezawa A, Ishida Y, Tateno C. Humanized liver mouse model with transplanted human hepatocytes from patients with ornithine transcarbamylase deficiency. J Inherit Metab Dis 2020 Dec 18. doi: 10.1002/jimd.12347. Online ahead of print.
- Fisher RA, Strom SC. Human hepatocyte transplantation: worldwide results. Transplantation 2006 Aug 27;82(4):441-9. doi: 10.1097/01.tp.0000231689.44266.ac.
- Enosawa S, Horikawa R, Yamamoto A, Sakamoto S, Shigeta T, Nosaka S, Fujimoto J, Nakazawa A, Tanoue A, Nakamura K, Umezawa A, Matsubara Y, Matsui A, Kasahara M. Hepatocyte transplantation using a living donor reduced graft in a baby with ornithine transcarbamylase deficiency: a novel source of hepatocytes. Liver Transpl. 2014 Mar;20(3):391-3. doi: 10.1002/lt.23800. Epub 2014 Feb 3.










