研究交流
小分子人工METアゴニスト(人工HGF)の創製
松本邦夫
金沢大学がん進展制御研究所
HGF(hepatocyte growth factor)はMET受容体を介して生理活性を発揮する(図1)。肝細胞選択的Met欠損マウス、傷害/病態モデル動物へのHGF投与の研究などから、HGF-Met系活性化が肝臓の再生・保護や線維化抑制につながることが明らかにされてきた(文献1)。現在、肝疾患や神経系の傷害・病態(脊髄損傷と筋萎縮性側索硬化症)を対象に組換えHGFタンパク質の臨床試験が進められている。また、HGF遺伝子を治療用物質とするHGF遺伝子治療の臨床試験も進められている。組換えHGFタンパク質、HGF遺伝子、いずれにおいても組織の再生を促し、組織や細胞の生存・保護につながる医薬として難治性疾患の治療に応用されることの意義は大きい。
HGFは697個ないしは692個のアミノ酸からなる糖タンパク質であり、サイトカイン/増殖因子の中では分子サイズの大きい生理活性タンパク質である。医薬候補としての組換えHGFの製造においては哺乳類細胞を宿主に発現される。HGFは本来、生体に存在している天然の生理活性分子であることが強みである一方、化学合成可能な小分子に比べると、製造コストやDrug Delivery技術との組合せなどによる汎用性向上などでは難点がある。私達は、最近、菅裕明教授(東京大学)らと共同で、化学合成可能な小分子人工METアゴニスト(人工HGF)の創製に成功した(Nat Commun, 6: 6373, 2015)(文献2)(図1)。
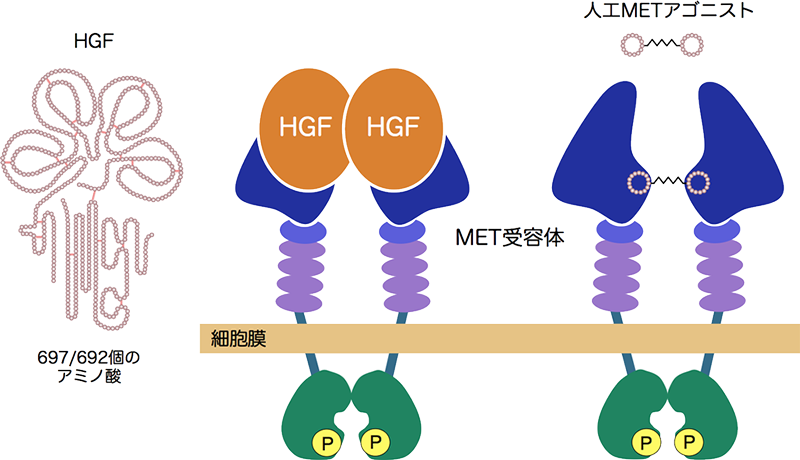
図1. HGFとMET受容体の概要と人工METアゴニストによるMET活性化の概要
HGFを含め細胞増殖因子は、受容体同士の2量体化を引き起こし、これによる相互チロシンリン酸化によってシグナル活性化に至る。したがって、MET受容体に高い親和性と選択性をもつ分子を創製し、その連結/2量体化によってHGFに置き換わる人工アゴニストの創製ができると予想される。ただし、予想は可能であるが、MET受容体に高親和性に結合する小分子を見出すことは極めて難しい。私達の研究で、MET受容体に対する小分子(特殊環状ペプチド)を取得する方法として用いられたのが、菅裕明教授らによって独自に確立されたRaPID(Random nonstandard Peptide Integrated Discovery)システムである。この手法は卓越した革新性をもっており、この手法によって取得される物質は、標的のタンパク質に高い親和性と特異性で結合する特殊環状ペプチドである(図2)。
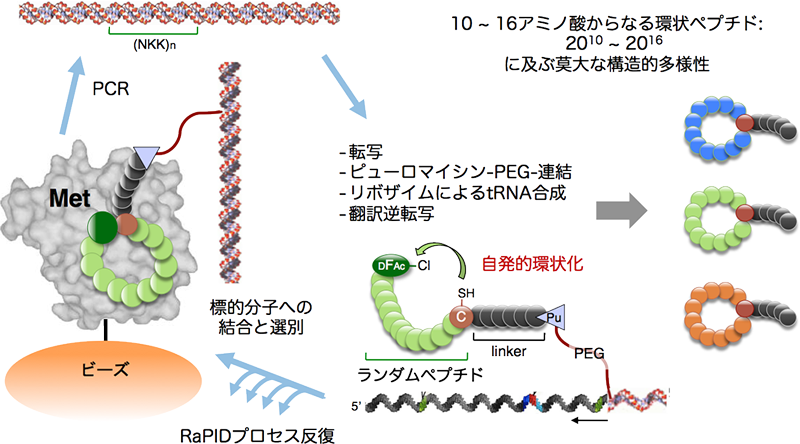
図2. RaPID法の概要
1つのアミノ酸を1つの構造単位とすると、仮に10個のアミノ酸がつながったペプチドの構造多様性は、アミノ酸を20種類とすると2010にも及び、膨大な多様性構造が生まれる。また、RaPID法ではtRNA合成酵素を使用せずにリボザイムが使用される。そのため化学修飾したアミノ酸、D型アミノ酸さえも部品としてペプチド内に取り込まれ、構造多様性がいっそう増す。莫大な構造多様性になるがゆえに、その中には目的のタンパク質に高親和性に結合するペプチドが必ず存在する。ランダムDNA配列からチューブ内無細胞系での転写・翻訳、ペプチドの自発的環状化反応、MET固相化ビーズによる環状ペプチド+DNA/RNA複合体回収、以上のサイクルを繰り返すことで標的タンパク質に結合する特殊環状ペプチドが得られる。
私達が得たMETアゴニストは13~15個のアミノ酸からなる特殊環状ペプチドを単鎖のポリエチレングリコールで連結したものであるが、HGFとは構造的な相同性はない。ダイマー化環状ペプチド(3種類)はいずれもMETに極めて高親和性に結合するとともに、MET受容体を選択的に活性化する。さらにいずれのダイマー化環状ペプチドもHGFタンパク質と同様、細胞増殖促進、細胞遊走促進、3-D上皮管腔形態形成誘導など多彩な活性を示し、しかもHGFと同等の最大活性を示した。化学合成可能な人工METアゴニストがあったら・・・、という思いは20年以上前からあったが、絵に書いた(憧れの)餅、であった。今回、 RaPID技術という卓越した技術を確立したチームとの共同研究の機会に恵まれ、天然のHGFに匹敵する人工METアゴニスト創製につながった。
化学合成可能な人工METアゴニストは、将来、Drug Delivery技術とのコンビネーション、低コストといった特性を活かした医薬候補になる可能性を秘めている。また、現在、iPS細胞をはじめ、細胞を使った再生医療が医療技術として急速に進展している。再生医療において大きな課題となるのがコストで、とりわけ無血清培養に必要な細胞増殖因子やサイトカインが高コストの要因となる。今回の研究によって、HGFに限らず、様々な人工サイトカインや人工細胞増殖因子を創製する普遍性の高い技術が確立された。したがって、特殊環状ペプチドによる人工サイトカイン/細胞増殖因子は、医薬候補としての応用に加え、再生医療における応用が期待される。
文献
- Sakai K, Aoki S, Matsumoto K. Hepatocyte growth factor and Met in drug discovery. J Biochem, 157: 271-284, 2015.
- Ito K†, Sakai K†, Suzuki Y, Ozawa N, Hatta T, Natsume T, Matsumoto K, Suga H. Artificial human Met agonists based on macrocycle scaffolds. Nat Commun, 6: 6373, 2015. (†equal contribution)










