研究交流
胆管系に分布する幹細胞 biliary tree stem cells
中沼安二
静岡がんセンター 病理診断科
はじめに
成体で、肝臓特異的な幹・前駆細胞が、胆管系の最末梢枝であるヘリング管(Canal of Hering)に存在すると考えられており、ヘリング管は解剖学的に肝内の小型門脈域の辺縁あるいはこれに接する肝小葉内に分布する(1)。ヘリング管に局在する組織幹細胞は肝細胞、胆管上皮細胞に分化でき、肝の再生や腫瘍を含めた種々の肝病態の形成に関係するとされている。最近、肝門部や肝外胆管系にも組織幹細胞の分布することが注目されており、この組織幹細胞(胆管系幹細胞 biliary tree stem cells, BTSC)は、胆管上皮、肝細胞、それに膵の細胞に分化するとされ、大型胆管を中心とした胆管の再生や病態形成、腫瘍形成への関与が注目され、研究が展開している(2)。
ここでは、最近、その存在が明らかになりつつある胆管系幹細胞(BTSC)の概要と今後の展望に関して述べる。
胆管系の解剖と胆管に分布する幹細胞BTSC
胆管系は、肝外胆管と肝内胆管から構成され、肝内胆管は、顕微鏡レベルの肝内小型胆管と肉眼レベルの肝内大型胆管に分類される。私どもの研究により、肝内大型胆管を含む肝門部胆管、胆嚢管、肝外胆管、Vater乳頭部の胆管には、胆管壁内外に腺組織が分布することが明らかとなり(3,4)、胆管周囲付属腺と呼ぶことを提唱してきた(図1)。胆管周囲付属腺は、壁内腺と胆管壁外の結合組織内に分布する壁外腺からなり、壁外腺は小葉状の構造を示し、固有の導管により、胆管内腔と連続する。壁外腺は漿液腺、粘液腺から構成され、頻度は低いが膵の外分泌腺房も介在している。ヒトやマウスでは、肝門部胆管で胆管周囲付属腺が、胆管壁内外で、互いに連続し、ネットワークを構成していることが最近報告されている(5,6)。最近、この付属腺に組織幹細胞/前駆細胞の分布することが報告された。
つまり、Cardinaleらは、ヒトの胆管付属腺上皮に前腸系の転写因子であるSOX9, SOX17, FOXA2, PDX1, HES1, NGN3, PROX1, SALL4や前腸系の幹細胞/前駆細胞の表面マーカーであるEpCAM, NCAM, CD133, CXCR4が発現していることを報告した(2)。しかし、成熟した肝細胞、胆管上皮、膵の遺伝子に関連する産物は殆ど発現しないとしている。そして、付属腺から胆管内腔に近づくに伴い、これらの細胞は分化することを報告している。また、肝内外胆管系の各レベルの胆管からの上皮細胞を、肝幹細胞や肝芽細胞用の培地(成熟した肝細胞や胆管上皮細胞は培養できない)で培養すると、前腸系の前駆細胞としての形質を示す上皮細胞が、未分化な状態で培養され、これらの細胞は、特に肝門部あるいは胆嚢頸部などの付属腺の密な部位からの培養で多く得られたことから、胆管周囲付属腺の細胞が培養されたとしている。そして、これらの培養細胞はヘテロの集団であり、培地中に添加するホルモンの種類や細胞外基質成分により、肝細胞(albumin, CYP3A4, transferrinを発現)、分枝を示す胆管上皮(anion exchanger-2やCFTRを発現)、それに膵のランゲルハンス島細胞(glucagon, insulinを発現)に分化することを報告した。これらのヒトの胆管周囲付属腺細胞を免疫抑制状態のマウスの肝臓に移植すると、肝細胞や胆管上皮の形態を示し、アルブミンやHepParIを発現し、またCK7を発現する胆管に分化することが示された。さらに、糖尿病マウスの脂肪組織に移植するとglucose-regulatable human C-peptideを分泌するランゲルハンス島になることを示した。つまり、微小環境に応じて、肝細胞、胆管細胞、さらには膵のランゲルハンス島細胞へ分化することが示された。すなわち、胆管周囲付属腺には、前腸系の組織幹細胞が分布し、胆管周囲付属腺の構造や機能を分子レベルで解明すれば、胆管の形成、維持、再生、さらには胆管系の疾患の解析が大きく進歩すると期待されている。
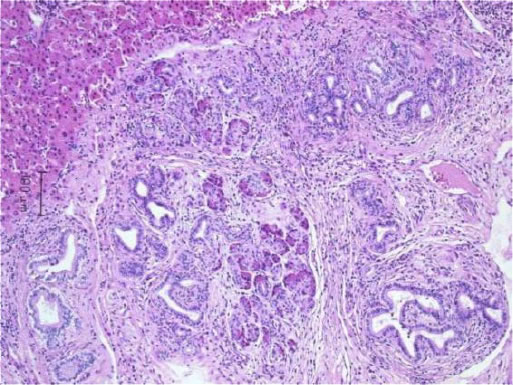
図1A:膵の腺房を有する付属腺
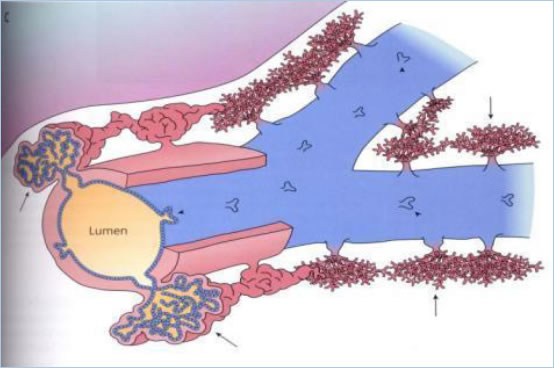
図1B:胆管周囲付属腺のシェーマ。
肝門部胆管周囲で付属腺がネットワークを形成している(文献5より引用)。
矢印は壁外腺、矢頭は壁内腺。
胆管系幹細胞の病的意義
それでは、胆管周囲付属腺に分布するこれらの組織幹細胞は、どのような役割を担っているのであろうか。現在、活発な研究が展開され、いくつかの生理的、病的意義が明らかになってきた。
胆管の再生: 胆管被覆上皮の障害後の胆管上皮再生に関して、胆管上皮自身の増殖、再生に加え、上皮障害が高度の場合、胆管周囲付属腺に分布する組織幹細胞が、胆管被覆上皮の再生に関連するとされている。また、肝移植に際し、移植されたドナー肝の胆管での付属腺および被覆上皮の障害状態を検討した結果、胆管壁の深部に分布する付属腺(壁外腺に相当)の障害が高度の症例では、移植後の胆管狭窄が発生しやすいことが最近、報告されている(7)。胆管周囲付属腺に存在する組織幹細胞が、肝細胞の再生や膵の再生や障害の修復に、どの様に関連するかに関しては、今後の検討課題である。
膵にカウンターパート疾患を伴う胆道系疾患:
従来より、胆管系に発生する腫瘍と膵に発生する腫瘍の類似性が注目されている。特に、乳頭状腫瘍である胆管内乳頭状腫瘍(IPNB)と膵での管腔内乳頭状粘液性腫瘍(IPMN), 嚢胞性腫瘍である肝の粘液性嚢胞性腫瘍(MCN)と膵のMCN, また胆管癌と膵管癌、およびその前癌病変である平坦な前浸潤性病変である胆管でのBilINと膵臓でのPanINの類似性が注目されている。私どもは、これらの疾患を“膵臓にカウンターパート疾患を伴う胆道系疾患”として提唱しているが、その機序として、胆管周囲付属腺に分布する膵と胆管に分化しうる組織幹細胞が、病態形成に参加している可能性があり、今後の検討課題と思われる(8,9)。
今後の展開
今回明らかとなった、胆管周囲付属腺に分布する組織幹細胞が、胆管、膵臓、肝臓の病態形成や修復にどの様な役割を演じているのか、今後の検討課題と思われる。
文献
- Kuwahara R, et al. The hepatic stem cell niche: identification by label-retaining cell assay. Hepatology. 2008;47(6):1994-2002. [PubMed]
- Cardinale V, et al. Multipotent stem/progenitor cells in human biliary tree give rise to hepatocytes, cholangiocytes, and pancreatic islets. Hepatology. 2011;54(6):2159-72. [PubMed]
- Nakanuma Y, et al. Microstructure and development of the normal and pathologic biliary tract in humans, including blood supply. Microsc Res Tech. 1997;38(6):552-70. [PubMed]
- Ishida F, Terada T, Nakanuma Y. Histologic and scanning electron microscopic observations of intrahepatic peribiliary glands in normal human livers. Lab Invest 1989;60(2):260-5. [PubMed]
- Nakanuma Y, Zen Y, Portman BC. Diseases of the bile ducts. In: MacSween’s Pathology of the Liver (Eds. Burt AD, Portman BC、Ferrell LD) Churchill Livingstone 6th ed., 2012 pp.491-562.
- Dipaola F, et al. Identification of intramural epithelial networks linked to peribiliary glands that express progenitor cell markers and proliferate after injury in mice. Hepatology. 2013; 58(4):1486-96. [PubMed]
- Op den Dries S, et al. Injury to peribiliary glands and vascular plexus before liver transplantation predicts formation of non-anastomotic biliary strictures. J Hepatol. 2014;60(6):1172-9. [PubMed]
- Nakanuma Y. A novel approach to biliary tract pathology based on similarities to pancreatic counterparts: is the biliary tract an incomplete pancreas? Pathol Int. 2010;60(6):419-29. [PubMed]
- Nakanuma Y, et al. Proposal of a new disease concept "biliary diseases with pancreatic counterparts". Anatomical and pathological bases. Histol Histopathol. 2014;29(1):1-10. [PubMed]










