研究交流
肝臓を構成する細胞の糖鎖認識
伊勢裕彦
東京工業大学フロンティア研究センター
肝臓は,肝機能の本質を担う肝実質細胞とこの肝実質細胞の増殖や生存を支える肝非実質細胞群により構成されている.肝非実質細胞は,肝星細胞(hepatic stellate cells)や類洞内皮細胞(sinusoidal endothelial cells),クッパー細胞(Kupffer cells)などから構成されており,細胞外マトリックスや増殖因子の産生を行い,肝細胞の生存や分化機能を維持している.近年,我々はこれらの肝臓を構成する細胞群が,ガラクトースとN-アセチルグルコサミン(GlcNAc)と呼ばれる糖にそれぞれ特異的な認識を持つことを見出した(図1).肝実質細胞は,古くからその細胞表面にアシアロ糖タンパク質レセプター(ASGP-R, asialoglycoprotein receptor)と呼ばれるガラクトースを認識するレセプターを持つことが知られている.このアシアロ糖タンパク質レセプターは,血中のシアル酸が欠如し末端にガラクトースが露出した糖鎖を有する糖タンパク質を肝細胞内に取り込み処理するという機能を有している.このようなことから,ガラクトースを有する高分子化合物や糖タンパク質を用いて肝細胞を特異的に認識する材料の設計が可能である.過去に赤池らは,肝細胞接着に対する特異的培養基材としてガラクトース結合ポリスチレン(PVLA, poly-[N-p-vinylbenzyl-O-4-β-D-galactopyranosyl-D-gluconamide]) を開発している1) (図1). PVLAは,ポリスチレン鎖にラクトースをグラフトした糖鎖高分子であり,側鎖の末端にガラクトースを有するので,ASGP-Rに非常によく認識される.またPVLAは,疎水性のポリスチレン鎖と親水性のラクトースから構成されている両親媒性の高分子であるので,疎水性のポリスチレン培養皿に対して強固な吸着が可能である.この性質を利用して,ポリスチレン培養皿にこのPVLAを吸着させた肝細胞特異的培養基材が開発された1) .そして,肝細胞を高機能に維持する培養器材としてガラクトースを有するPVLAを利用した肝細胞の培養系と様々な機能制御を報告してきた2).
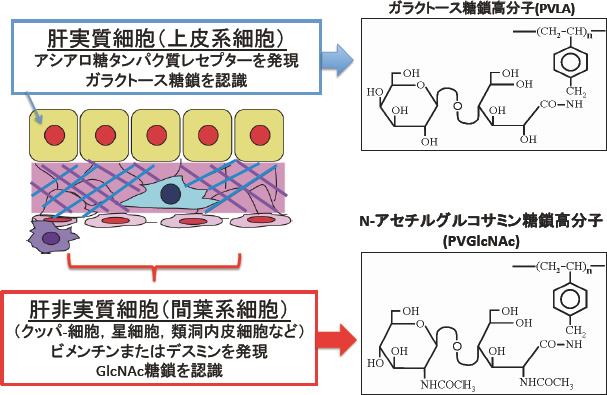
図1 肝臓構成細胞の糖鎖認識
そこで本章では星細胞を含む肝非実質細胞認識材料としてPVGlcNAcに住目いたしました。肝臓のそれぞれの細胞は発現しているタンパク質マーカも違うことが報告されています。
hepatocyteはASGPR陽性vimentin陰性であり非実質細胞はvimentin陽性ASGPR陰性であります。そこで私は従来遠心方で行った肝細胞の分離をASGPR 認識高分子PVLAとvimentin認識高分子を用いることで試みました。
一方で近年,伊勢らはGlcNAcを末端に持つ糖鎖高分子PVGlcNAc (poly[N-p-vinylbenzyl-O-2-acetoamid-2-deoxy-β-D-glucopyranosyl-(1→4)-2- acetoamide-2-deoxy-β-D-gluconamide])が間葉系細胞や骨格系細胞において高い相互作用を持つことを明らかにした(図1,2).このPVGlcNAcへ相互作用は,細胞骨格分子であるビメンチンやデスミンが細胞表面に出現し,GlcNAc結合性のレクチン活性を有することで行われていることを明らかにしている3).細胞骨格分子であるビメンチンやデスミンが,細胞表面に発現しGlcNAc結合活性を持つことは,今までに報告されたことはなく, PVGlcANcのような糖鎖高分子によってはじめて明らかにされた興味深い事実である.
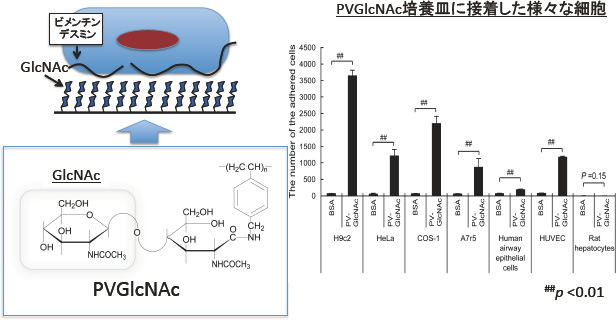
図2 GlcNAc糖鎖高分子PVGlcNAcの様々な細胞に対する相互作用
近年、我々はN-アセチルグルコサミン(GlcNAc)を有する糖鎖高分子PV-GlcNAcが、心筋細胞や血管平滑筋細胞をなどの骨格系や間葉系の細胞に対して高い相互作用を示すことを見出した。
これは、PV-GlcNAcコーティング培養皿に対する様々な細胞の接着性を見た物であるが、HeLa細胞や心筋系、骨格系の培養細胞が高い接着性を持つことを明らかにした。
一方、初代培養の気道上皮細胞や肝細胞などの上皮細胞は、相互作用を示さないことが明らかになった。
そこで、細胞表面にGlcNAcを認識するレクチンの存在を推測し、GlcNAc結合性のれくちんをPV-GlcNAcを用いて、探索したところ意外なことに細胞骨格分子として知られているビメンチンやデスミンが細胞外に出現しGlcNAc結合活性を有していることが明らかになりました。
最近,筆者らはこのPVGlcNAcがビメンチンやデスミンを発現する肝非実質細胞や繊維芽細胞に対する特異的な培養基材になることを報告した4).肝非実質細胞は,類洞内皮細胞や星細胞,クッパー細胞より主に構成されており,これらの細胞は間葉系細胞に属することから細胞骨格分子であるビメンチンやデスミンを発現することが知られている.一方,肝細胞は上皮系に属する細胞集団であるため,ビメンチンやデスミンを発現しておらずPVGlcNAcには相互作用しない.そこで,筆者らは,PVLAとPVGlcNAcコート培養皿を用いて肝細胞及び肝非実質細胞の選択的な培養が可能か検討した(図3).その結果,PVLAに接着した細胞は,94%以上が上皮細胞のマーカーであるサイトケラチンが陽性であり,ほとんど肝細胞が接着していることが示された.一方,PVGlcNAc上の細胞では92%以上が,ビメンチン及びデスミン陽性の細胞であった.このことから,PVLAとPVGlcNAcを用いることで,肝臓細胞の選択的な培養が実現できることが示された(図3).特に肝星細胞はビメンチンとデスミンを発現しているためPVGlcNAcに対する高い接着が観察された.著者らは,ガラクトースを有する糖鎖高分子PVLAとGlcNAcを有する糖鎖高分子PVGlcNAcの2種類を用いる事で肝実質細胞と肝非実質細胞の機能制御に成功した(図4)4).肝臓細胞を2種類の糖鎖によって機能制御できるという発見は肝臓細胞の生体外での機能制御として非常に興味深い.これらの知見から,ガラクトースとGlcNAcの二種類の糖をパターニングした培養基質を利用すれば,肝実質細胞と肝非実質細胞を制御した共培養系の構築が可能になり,肝実質細胞の高機能を維持した機能制御が実現できるであろう.
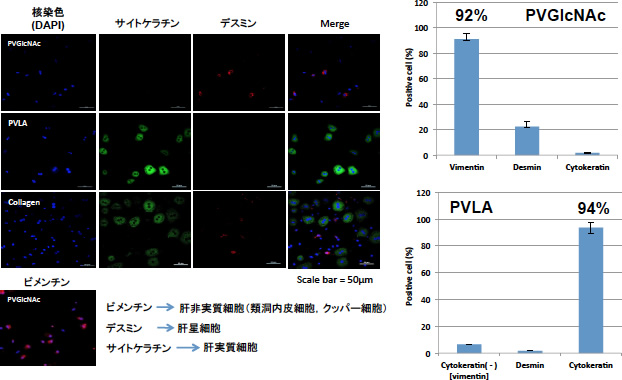
図3 各種糖鎖高分子培養皿に接着した細胞の免疫染色
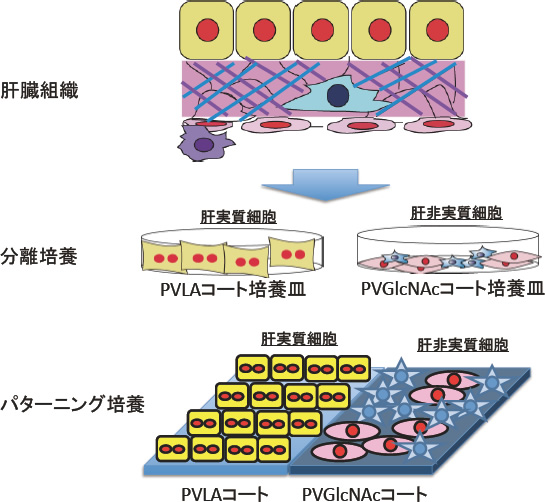
図4 ガラクトース及びGlcNAc糖鎖高分子による肝臓構成細胞の機能制御
参考文献
- Kobayashi K et al; Culturing hepatocytes on lactose-carrying polystyrene layer via asialoglycoprotein receptor-mediated interactions. Methods Enzymol. 247:409-18, 1994
- Cho CS et al; Galactose-carrying polymers as extracellular matrices for liver tissue engineering. Biomaterials 27:576-585, 2006
- Ise H et al; Vimentin and desmin possess GlcNAc-binding lectin-like properties on cell surfaces. Glycobiology 20:843-864, 2010
- Kim SJ et al; Interactions of vimentin- or desmin-expressing liver cells with N-acetylglucosamine-bearing polymers. Biomaterials 33:2154-2164, 2012










