研究交流
成人肝上皮性細胞株の分化能
常盤孝義
(財)河野臨床医学研究所 肝細胞学研究室
要旨
正常ヒト肝上皮性細胞がSV40-Large 抗原遺伝子により不死化され、THLE-5b細胞株が樹立された。THLE-5bは、染色体上異数性であるが、造腫瘍性は認められていない。THLE-5bは、また、オーバル細胞 (oval cell) あるいはある種の肝上皮性細胞 (LEC) に共通する形質を発現するとともに、分化能を有することが旋回培養法あるいは動物への移入実験によって明らかとなった。これらは、THLE-5bが肝プロジェニター様細胞の性質を有することを示唆するものである。
はじめに
哺乳動物肝臓はさまざまな生理病理的環境の下で、肝幹あるいはプロジェニター様細胞の増殖、分化による高い再生能力を示すことが知られている。動物モデルの研究から、肝幹様細胞の性質を示す細胞として、オーバル細胞が知られている1。肝上皮性細胞は正常肝組織の培養で認められ、肝幹あるいはプロジェニター様細胞の性質を示すものがある2-4。オーバル細胞は細胞株としても樹立されているが、肝上皮性細胞の細胞株は少ない。THLE-5bは成人肝上皮性細胞に由来する不死化細胞株である5-11。THLE-5bが肝幹あるいはプロジェニター様細胞の性質を示すかどうかは興味ある課題である。本稿では、THLE-5bの形質発現と分化能について概説する。
THLE-5bの樹立
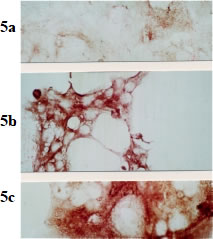 図1.不死化で生じた3種のコロニー(5a, 5b, 5c) のCK18免疫染色。THLE-5bは5bに由来する。(Tokiwa ら、未発表データー) |
THLE-5bはアメリカ合衆国国立癌研究所において筆者らにより樹立された5,11。樹立過程の概略は以下のとおりである。ヒト肝組織(剖検材料)の小片を0.05%コラーゲナーゼ灌流し、低速遠心後、主として非肝実質細胞からなる分画を初代培養した。上皮性細胞を認めた時点で、SV40-Large 抗原遺伝子の導入による不死化操作を試みた。培養30日頃、コロニー性の増殖を示す3種の細胞 (5a,5b,5c) (図1)を認めたので、それぞれをクローニングした。THLE (Transformed Human Liver Epithelial Cells)-5bと命名された細胞株は5b細胞に由来する。
THLE-5bは低密度培養では、紡錘型形態を示し、高密度培養では、敷石様形態を示した。いずれにおいても上皮性細胞のマーカーCK18は陽性であった。樹立当初、同細胞株の細胞生物学的性質は、異数性染色体;軟寒天内非コロニー形成;ヌードマウス不可移植性などであり、トランスフォームはしているが非腫瘍であると判定された。これらの性質は50継代後の現在、維持されている。
THLE-5bの形質発現
THLE-5bの発現マーカーを、肝幹あるいはプロジェニター様細胞の観点から精査し、肝幹あるいはプロジェニター様細胞の性質を示すヒト3あるいはブタ2,4 肝上皮性細胞(いずれも初代培養細胞)ならびにオーバル様細胞株HepaRG 12と比較した(表1)。その結果、THLE-5b は肝上皮性細胞ならびにHepaRGのいずれか一方、あるいは共通に認められるマーカーを多数発現していた。一般的に、肝幹あるいはプロジェニター様細胞の性質を有する肝上皮性細胞とオーバル細胞は、共通のマーカーを有し、区別が困難であると言われる。本結果は、THLE-5bが少なくとも肝プロジェニター様細胞の性質を有することを示唆するものである。
表1 肝幹あるいはプロジェニター細胞マーカーによる THLE-5b とLEC(肝上皮性細胞)あるいはHepaRG (オーバル様細胞株)の比較
| αfetoprotein | Albumin | CK14 | CK18 | CK19 | OV6* | Vimentin | Thy-1 | |
| THLE-5b7,10) | – | –⁄ ± | + | + | + | NT | + | + |
| LEC3)(human) | + | + | NT | + | + | + | NT | + |
| LEC2,4)(pig) | + | + | NT | + | – | + | + | + |
| HepaRG 12) | NT | – | NT | + | + | + | – | NT |
–、陰性; ±、弱陽性; +、陽性; NT、未検。
*OV6抗体はCK14とCK19に反応する。
THLE-5bの分化能
THLE-5bの分化能の検出は、細胞凝集塊を形成させる方法によった。単層培養され、コンフルエント(Confluent, Conf)となったTHLE-5bと同細胞をフラスコに播種後、生じた凝集塊 (Aggregate, Agg) の形質発現を比較した7。凝集塊形成は、無血清培養下、1)フラスコを非細胞接着性のpoly-(2-hydroxyethylmethacrylate, HEMA) でコートし、静置培養する (Agg-1);2) poly-HEMAでコートし、旋回培養する (Agg-2);3) siliconでコートし、旋回培養する (Agg-3) の三条件によった。1) 細胞凝集塊:Agg-1の凝集塊は、Agg-2やAgg-3のコンパクトなそれと異なり、ルーズな細胞集団であった。2) 形質発現:Tryptophane 2,3-dioxygenaseなどの成熟肝細胞のマーカーとされるいくつかの遺伝子発現を調べた。その結果、Agg-2あるいはAgg-3において高いレベルでの遺伝子発現を認めた(図2)。Agg-1における発現レベルは、単層培養のそれとほぼ同レベルであった。これはAgg-1が肝幹あるいはプロジェニター様細胞を選択する培養条件となる可能性を示唆するものである。事実、THLE-5bは長期の無血清培養(EGFやbFGFなどの因子を添加)において神経幹細胞などで認められているスフェアを形成した(未発表)。凝集塊 (Agg-3) の超微細構造については、肝細胞に特徴的な毛細胆管様構造や密着結合を認めた7。さらに、肝細胞機能を示すアンモニア代謝活性もまた凝集塊において有意に増加していた7。
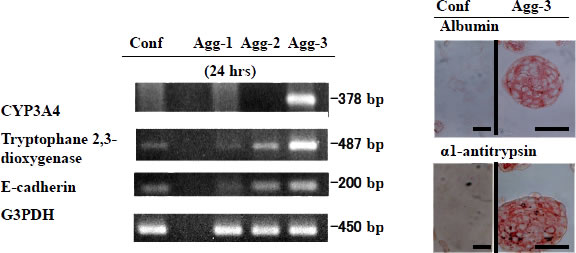
図2. THLE-5bの分化能の検討。 細胞凝集塊を形成させ、分化能を検討した。THLE-5b はAgg-2,-3 において成熟肝細胞のマカーを強く発現した。 Conf, Confluent; Agg, Aggregate.
Bar, 25μm (文献 7より一部改変)
動物体内での分化能の検討のため、THLE-5bを、ビーズ培養し、そのまま動物 (severe combined immunodeficient mice, SCID) 腹腔に移入した。3週後、体内から回収した細胞において、単層培養ではほとんど認められないAlbumin やα1-antitrypsin の強い発現を認めた(図3)。一方、CK19の発現は認められなかった。
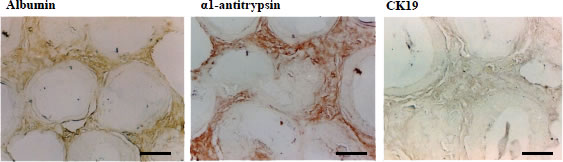
図3.SCID mouse腹腔 に移入されたTHLE-5b。 ビーズの周辺に albumin, α1-antitrypsin 陽性、CK19 陰性の細胞が認められる。Bar, 25 μm (文献 7 より)
以上の結果は、THLE-5bが肝プロジェニター様細胞として、少なくとも成熟肝細胞様細胞の方向への分化能を有することを示唆するものである。
おわりに
初代培養細胞と異なり、不死化細胞は細胞株としてほぼ無制限の増殖を示す。また、形質は比較的安定に保持され、かつ凍結保存が可能なため、反復実験が可能である。最近、筆者らは同細胞株から分離されたside population (SP) 細胞に関する研究でもTHLE-5bが肝幹あるいはプロジェニター様細胞の性質を有することを示唆する結果を得た8,10。非腫瘍性のTHLE-5bは肝細胞癌化や肝再生機構に関するさまざまな基礎的研究に利用可能と考える。
文献
- Grisham JW, Thorgeirsson SS (1997) Liver stem cells. In: Potten CS, ed. Stem cells. London: Academic Press; 233-282.
- Kano J, Noguchi M, Kodama M, Tokiwa T (2000) The in vitro differentiating capacity of nonparenchymal epithelial cells derived from adult porcine livers. Am J Pathol 156: 2033-2043.
- Khuu DN, Najimi M, Sokal E (2007) Epithelial cells with hepatobiliary phenotype: Is it another stem cell candidate for healthy adult human liver? World J Gastroenterol 13: 1554-1560.
- Tokiwa T, Yamazaki T, Ono T et al (2008) Cloning and characterization of liver progenitor cells from the scattered cell clusters in primary culture of porcine livers. Cell Transplant 17: 179-186.
- Lechner JF, Smoot DT, Pffeifer AM, Tokiwa T et al (1990) A non-tumorigenic human liver epithelial cell culture model for chemical and biological investigations. In: Rhim JS, Drifschlo A eds. Neoplastic transformation in human cell system. Mechanism of carcinogenesis. NY: Humana Press; 307-321.
- Tokiwa T, Kano J, Noguchi M et al (1998) Restoration of differentiated functions in multicellular aggregates of a human liver epithelial cell line. Mat Sci Engineer 6: 249-252.
- Tokiwa T, Yamazaki T, Xin W et al (2006) Differentiation potential of an immortalized non-tumorigenic human liver epithelial cell line as liver progenitor cells. Cell Biol Int 30: 992-998.
- Yamazaki T, Enosawa S, Tsukiyama T, Tokiwa T (2008) Presence of side population cells in an immortalized nontumorigenic human liver epithelial cell line. In Vitro Cell Dev Biol 44: 6-9.
- Tokiwa T, Yamazaki T, Tsukiyama T (2008) Evidence supporting the existence of liver progenitor cells in human livers. In: Bursides WB, Ellsley RH eds. Stem cell applications in disease and health. NY: Nova Publishers; 7-16.
- Tokiwa T, Yamazaki T, Enosawa S (2011) Side population cells from an immortalized human liver epithelial cell line exhibit hepatic stem-like properties. Cell Medicine (in press).
- Tokiwa T, Lipsky MM, Smoot DT et al (1994) A method for transforming human liver epithelial cells by transfection using a plasmid containing SV40 early region gene. J Tissue Culture Methods 16: 57-60.
- Parent R, Marion M-J, Furio L et al (2004) Origin and characterization of a human bipotent liver progenitor cell line. Gastroenterology 126: 1147-1156.










